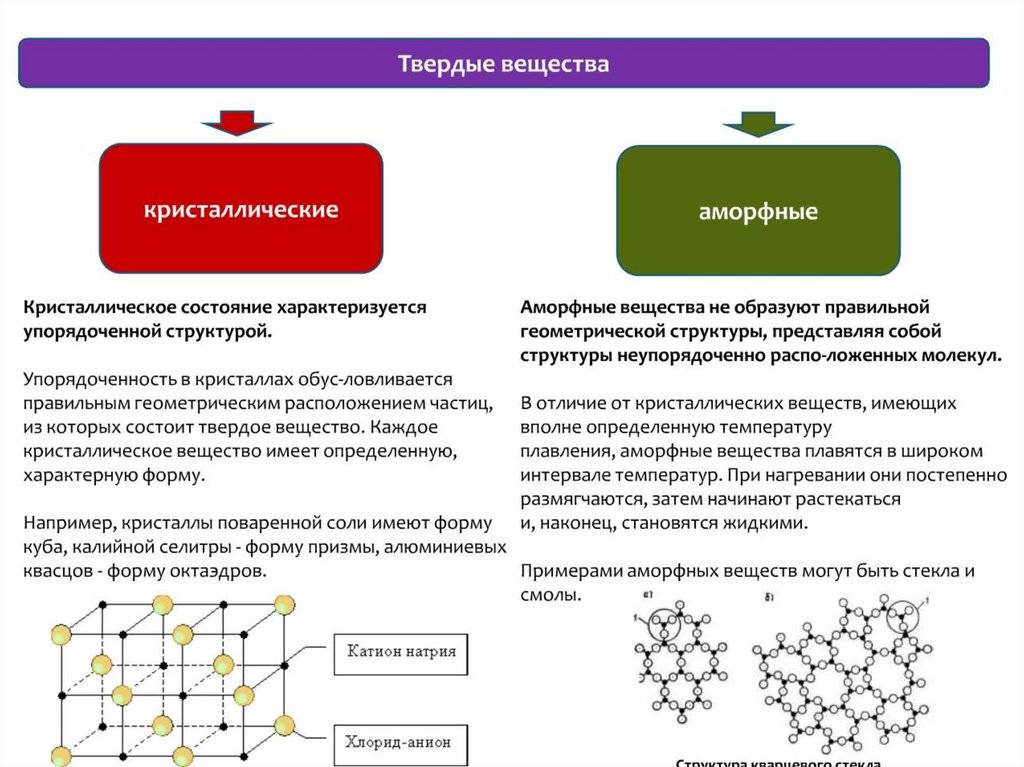
Твердые тела
Все твердые тела обладают следующими общими свойствами:
- Способностью долгое время сохранять форму и объем (геометрические размеры);
- Наличием упругих сил, которые возникают при небольших изменениях объема от внешнего воздействия (сжатия, растяжения или сдвига).
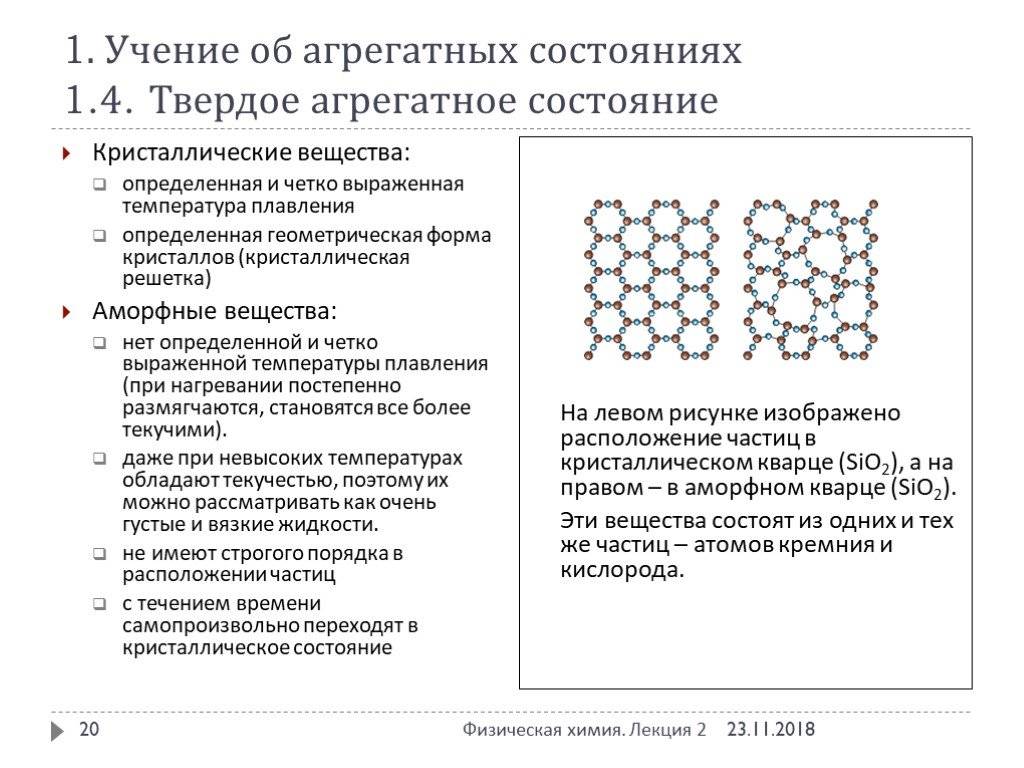
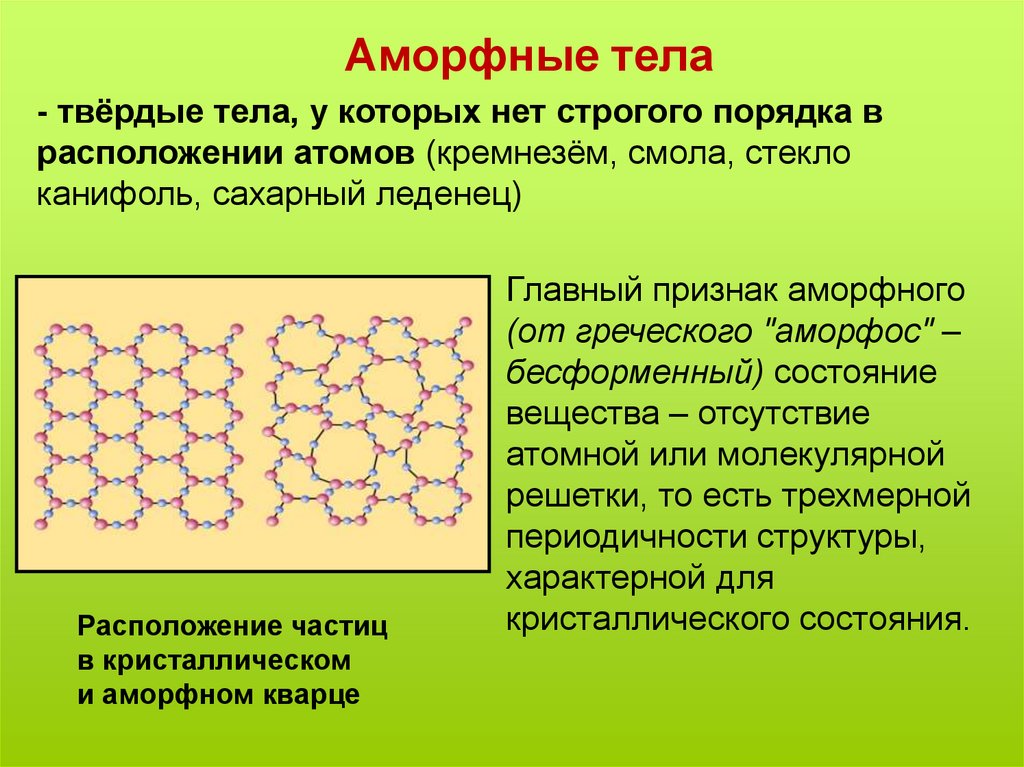
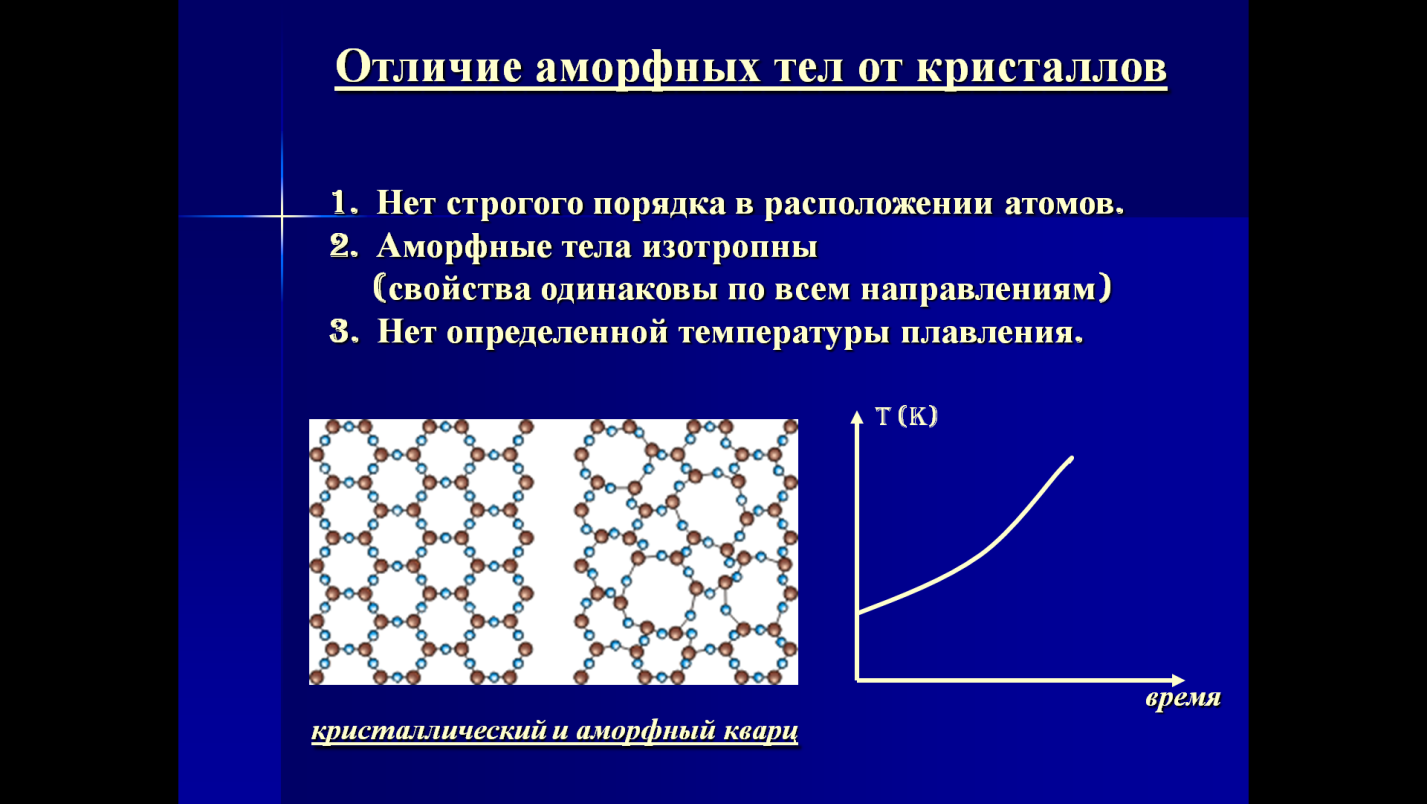
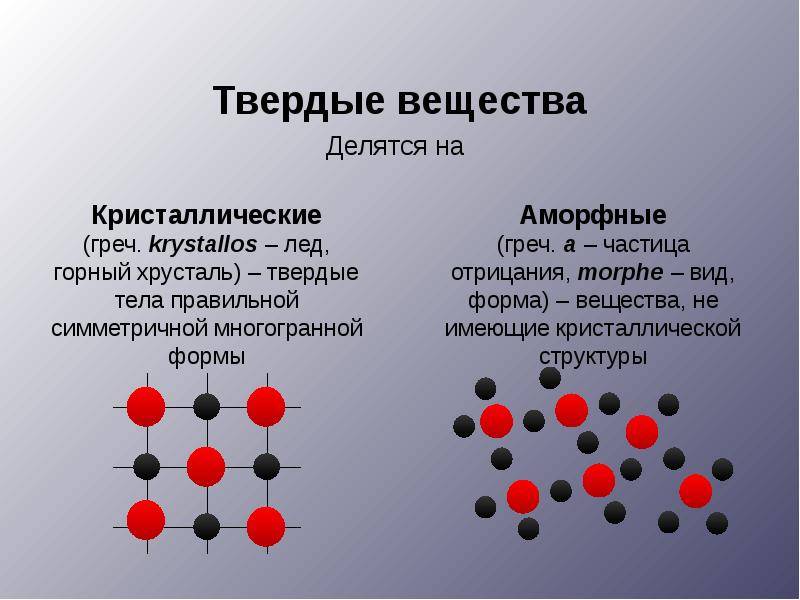
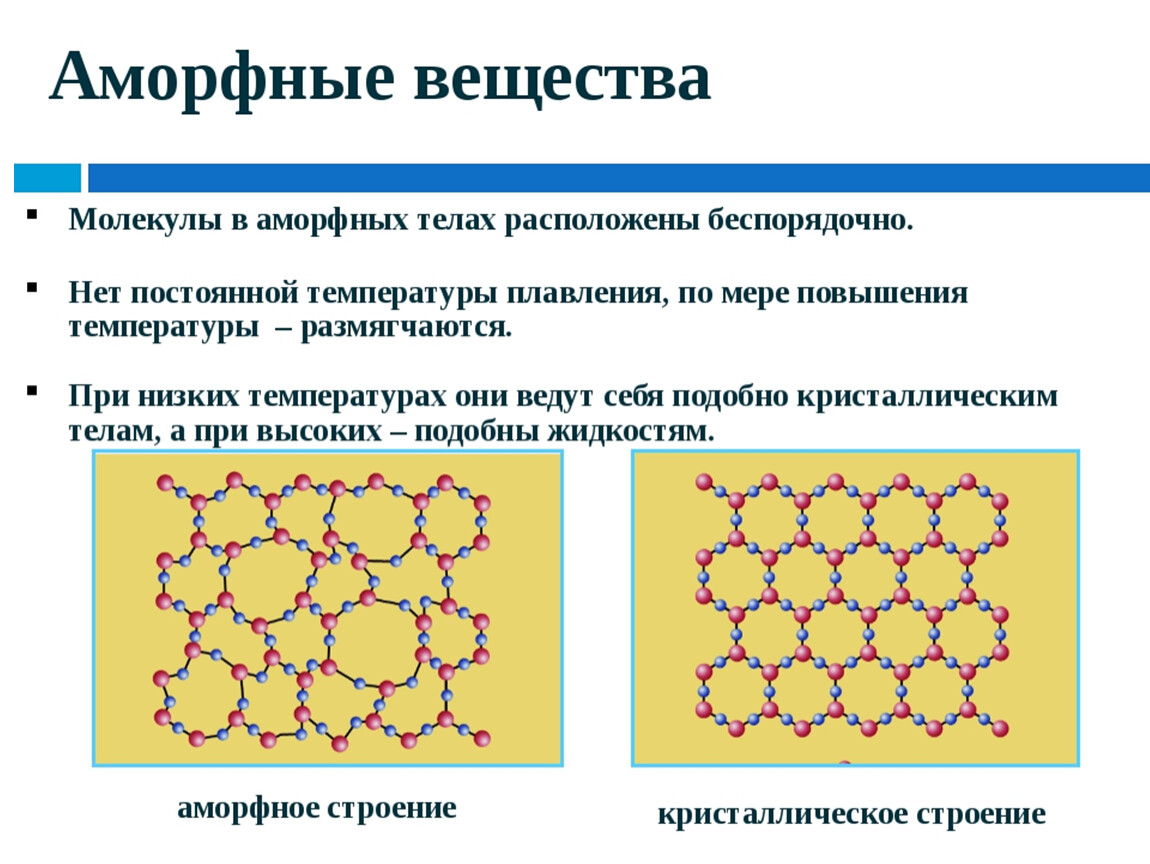
Рис. 1. Примеры решеток кристаллических и аморфных тел – кварц аморфный и кристаллический.
Современные ученые исследуют пространственное расположение атомов и молекул в твердых телах с помощью электронных микроскопов, которые позволяют получить изображение объекта с сильным увеличением (до 106 раз). Первый электронный микроскоп был изобретен в 30-х годах прошлого века. В 2018 г. с помощью последних версий этого прибора было получено разрешение 0,39 ангстрем. Напомним, что 1 ангстрем равен 10-8 см. В большинстве кристаллов это соответствует шагу атомной решетки.
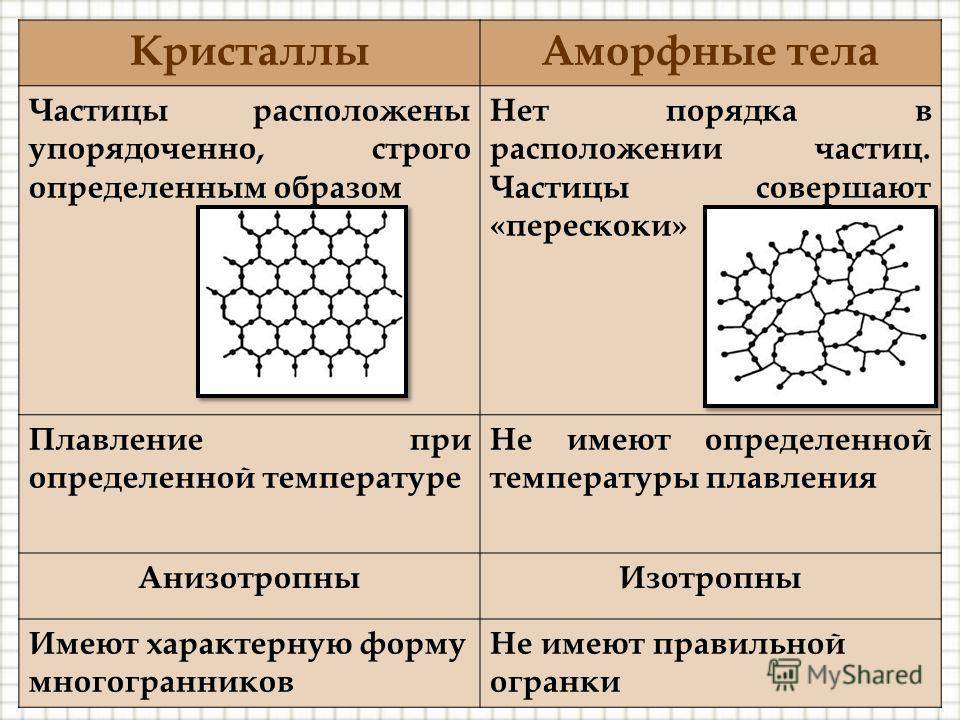
Отличия от кристаллических
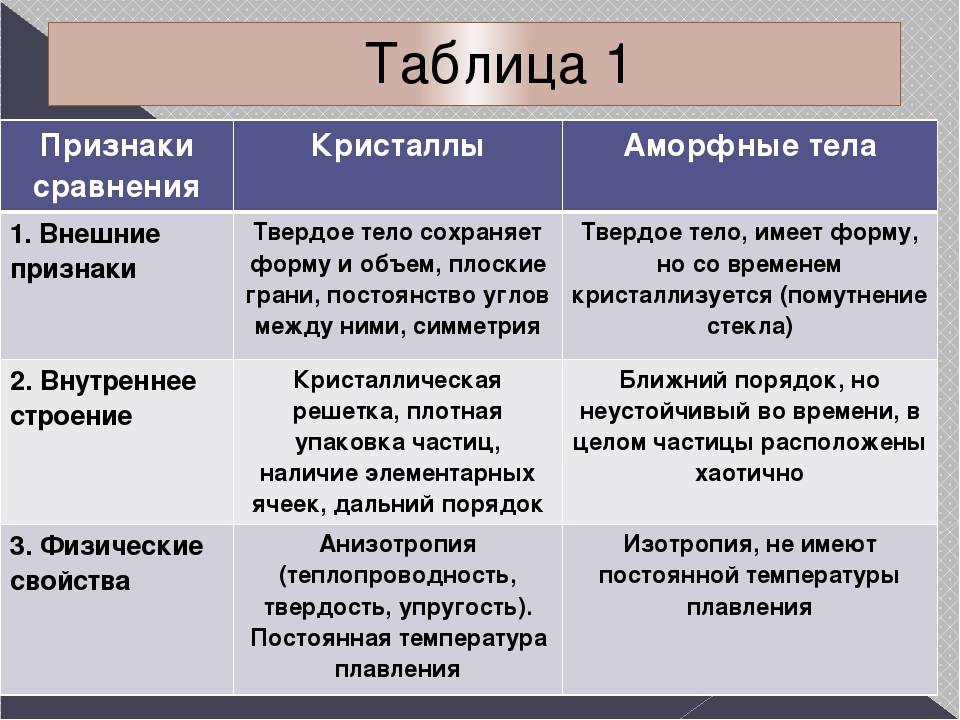
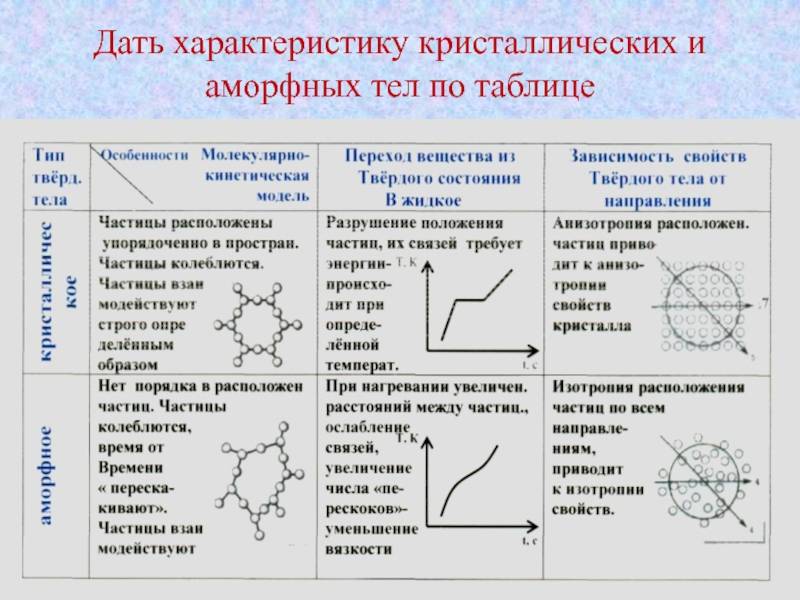
Твердые аморфные вещества отличаются от твердых кристаллических веществ по ряду характеристик:
| Характеристика | Твердые аморфные вещества | Твердые кристаллические вещества |
| Структура | Не имеют четкой и регулярной решетки | Имеют четкую и регулярную решетку |
| Форма | Могут иметь форму аморфных капель, пленок или порошка | Имеют определенные геометрические формы (кристаллы) |
| Оптические свойства | Могут быть прозрачными, мутными или полупрозрачными | Могут быть прозрачными или мутными, но обладают определенным показателем преломления |
| Теплопроводность | Могут обладать низкой теплопроводностью | Обычно обладают высокой теплопроводностью |
| Химическая стабильность | Могут быть менее химически стабильными | Чаще всего обладают высокой химической стабильностью |
Твердые аморфные вещества обладают более случайной и беспорядочной структурой, в отличие от твердых кристаллических веществ, которые образуют регулярные кристаллические решетки. Это делает аморфные вещества более уникальными и сложными для изучения и моделирования. Кристаллические вещества, в свою очередь, имеют более организованную структуру и обладают рядом характеристик, связанных с периодичностью решетки, таких как оптические свойства и форма кристаллов.
Характеристики твердых элементов
Вот некоторые из наиболее распространенных характеристик твердых элементов:
1 – У них есть частицы с низкой кинетической энергией (энергия, получаемая от движения), потому что близость между этими частицами мешает им двигаться.
2 – Электроны атомов, составляющих твердые тела, находятся в движении, что вызывает небольшие колебания. Тем не менее, атомы остаются фиксированными на месте.
3 – Твердые частицы имеют определенную форму, что означает, что они не принимают форму контейнера (как, например, с жидкостями).
4 – Они имеют определенный объем.
5 – частицы твердого вещества настолько объединены, что увеличение давления не уменьшит объем твердого тела при сжатии.
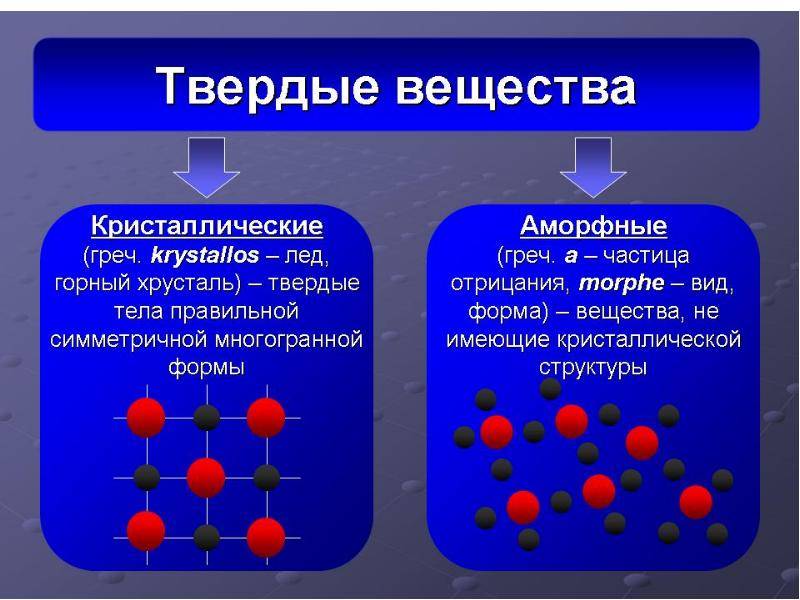
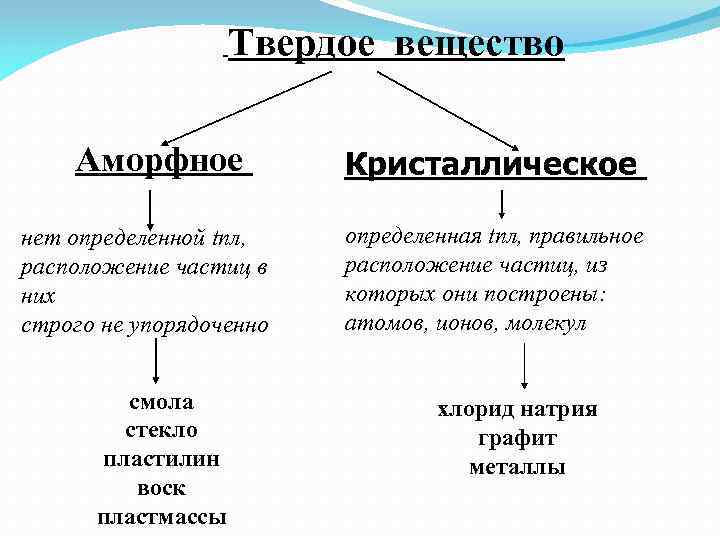
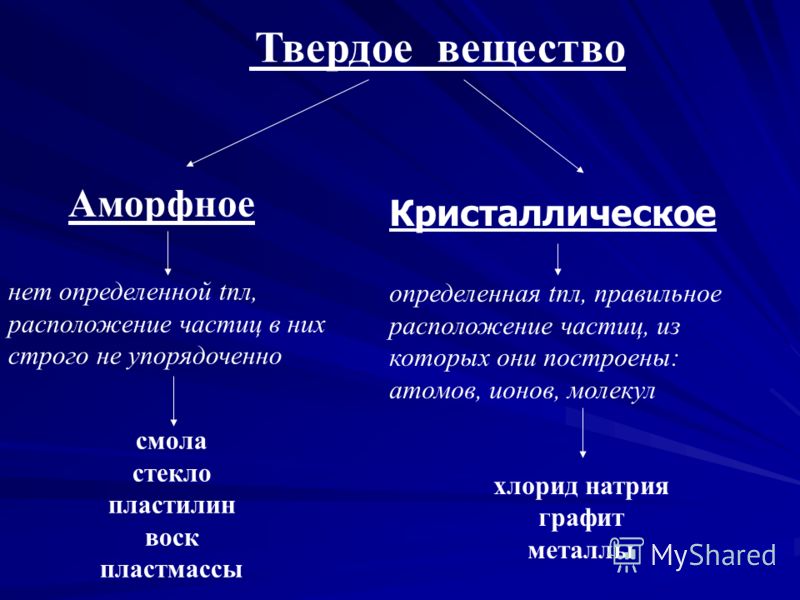
Твердые вещества делятся на две основные категории в зависимости от того, как частицы, которые их образуют, организованы: кристаллические и аморфные твердые вещества..
В кристаллических твердых телах, которые иногда считаются настоящими твердыми, атомы и молекулы организованы по симметричной и повторяющейся схеме. Эти твердые вещества, в свою очередь, могут быть четырех типов:
ионный, состоит из ионов противоположных зарядов: аниона (ион отрицательного заряда) и катиона (ион положительного заряда). Они могут растворяться в воде и проводить электричество.
молекулярная, состоит из молекул с ковалентными связями (то есть связей, в которых электроны являются общими). Некоторые из них могут быть растворены в воде, а другие нет. Следует отметить, что молекулярные твердые вещества не являются проводниками электричества.
Ковалентная сеть, в этих твердых телах нет отдельных молекул, что означает, что атомы соединены ковалентными связями в непрерывную цепь, которая приводит к большому кристаллу. Они очень твердые, не растворяются в воде и не проводят электричество.
металл, Это непрозрачные, глянцевые, податливые (могут быть сформированы в листы) и пластичные (могут быть отформованы для создания кабелей). В целом, они имеют удивительно высокую температуру плавления.
С другой стороны, в аморфных твердых веществах, также называемых псевдозолидами, частицы, которые их образуют, не следуют определенному образцу, отсюда и название «без формы»..
Они не имеют определенной температуры плавления, но постепенно сливаются, так как связывающие их соединения не разрушаются одновременно (как воск плавления свечи)..
ссылки
- Бэгли, Мэри (2016). Материя: определение и пять состояний материи. Получено 23 мая 2017 г. с сайта livescience.com
- Бэгли, Мэри (2014). Свойства вещества: твердые тела. Получено 23 мая 2017 г. с сайта livescience.com
- Перечислите 10 видов твердых веществ, жидкостей и газов. Получено 23 мая 2017 г.
- Примеры твердых веществ, жидкостей и газов. Получено 23 мая 2017 г.
- Твердое вещество. Получено 23 мая 2017 г. с сайта en.wikipedia.org
- Какие примеры твердых веществ? Получено 23 мая 2017 г. с сайта quora.com
- Твердые вещества, жидкости и газы. Получено 23 мая 2017 г. с сайта myschoolhouse.com
Механические свойства кристаллических твердых тел
Кристаллические твердые тела обладают уникальными механическими свойствами, которые определяются их кристаллической структурой и взаимной ориентацией атомов. Вот некоторые из основных механических свойств кристаллических твердых тел:
- Твердость. Кристаллические твердые тела могут быть очень твердыми, что делает их устойчивыми к царапинам и истиранию. Твердость зависит от межатомного расстояния и типа связей между атомами в кристаллической структуре.
- Прочность. Кристаллические твердые тела обладают высокой прочностью, что означает их способность сопротивляться деформациям под воздействием механических сил. Прочность зависит от типа и структуры кристаллической решетки.
- Упругость. Кристаллические твердые тела могут иметь хорошую упругость, что позволяет им возвращаться к исходной форме после применения механических сил. Упругость зависит от связей между атомами в кристаллической структуре.
- Ломкость. Кристаллические твердые тела могут обладать как хрупкостью, так и пластичностью при ломке. Хрупкие материалы ломаются без деформации, в то время как пластичные материалы могут быть деформированы без окончательной ломки.
Механические свойства кристаллических твердых тел являются результатом сложной взаимосвязи атомов и их ориентации в кристаллической структуре. Эти свойства делают кристаллические материалы важными в различных областях науки и техники, включая строительство, электронику, металлургию и многое другое.
Свойства аморфных тел
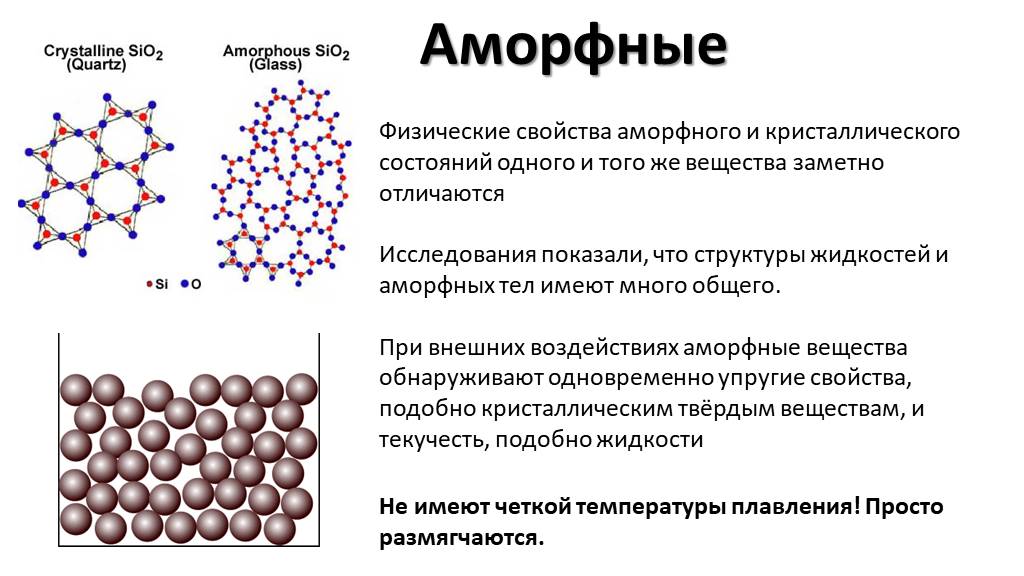
Все аморфные тела изотропные, т.е. их физические свойства одинаковы по всем направлениям. К аморфным телам относятся стекло, смола, канифоль, сахарный леденец и др.
При внешних воздействиях аморфные тела обнаруживают одновременно упругие свойства, подобно твёрдым телам, и текучесть, подобно жидкости. Аморфное тело обладает слабо выраженной текучестью. Так, если воронку наполнить кусочками воска, то через некоторое время (различное для разных температур) кусочки воска будут “расплываться”. Воск примет форму воронки и начнет “вытекать” из нее.
Аморфные тела при низких температурах по своим свойствам напоминают твёрдые тела. Текучестью они почти не обладают, но по мере повышения температуры постепенно размягчаются и их свойства всё более и более приближаются к свойствам жидкостей. Это происходит потому, что с ростом температуры постепенно учащаются перескоки атомов из одного положения в другое. Определённой температуры плавления у аморфных тел, в отличие от кристаллических, нет. Вещество в аморфном состоянии при нагревании постепенно размягчается и переходит в жидкость (рис. 8, кривая 2). Вместо температуры плавления приходится говорить о температурном интервале размягчения.
Жидкие кристаллы
Жидкие кристаллы — вещества, обладающие одновременно свойствами как жидкостей (текучесть), так и кристаллов (анизотропия).
По структуре они представляют собой жидкости, похожие на желе, состоящие из молекул вытянутой формы, определённым образом упорядоченных во всем объёме этой жидкости (рис. 10).
Рис. 10
Жидкие кристаллы — это почти прозрачные субстанции, проявляющие одновременно свойства кристалла и жидкости. Их внешнее состояние при нагревании может изменяться от твердого до жидкокристаллического и полностью переходить в жидкую форму при дальнейшем повышении температуры.
Жидкие кристаллы открыл в 1888 г. австрийский ботаник Ф. Рейнитцер
Он обратил внимание, что у кристаллов холестерилбензоата и холестерилацетата было две точки плавления и, соответственно, два разных жидких состояния — мутное (от 145 °С до 179 °С) и прозрачное (выше 179 °С). Однако, учёные не обратили особого внимания на необычные свойства этих жидкостей
Долгое время физики и химики в принципе не признавали жидких кристаллов, потому что их существование разрушало теорию о трёх состояниях вещества: твёрдом, жидком и газообразном.
Монокристаллы и поликристаллы
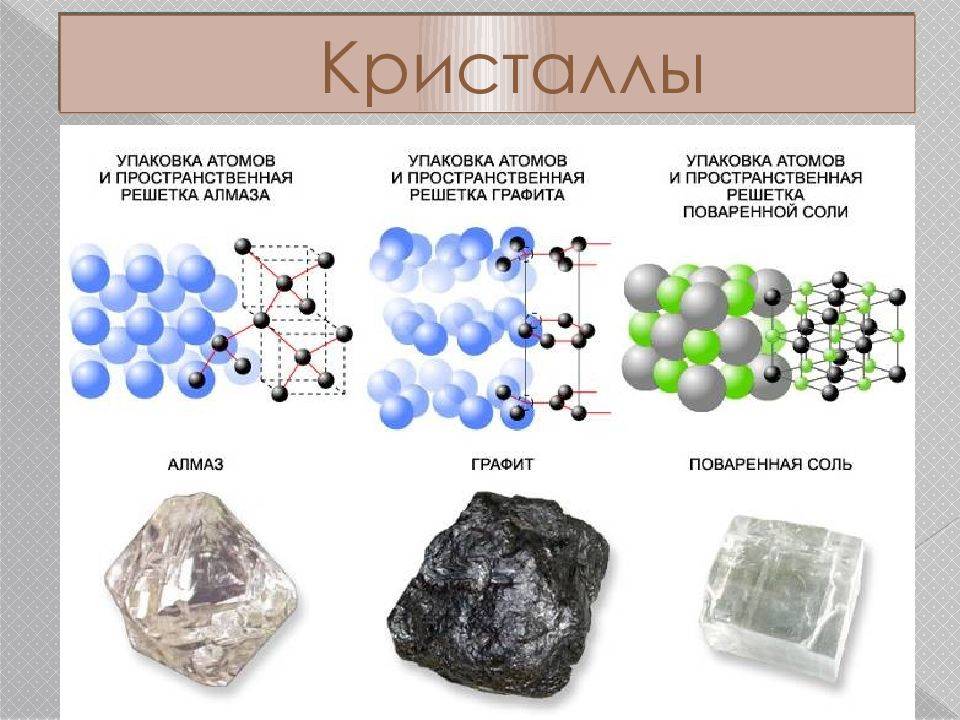
Если периодически повторяющаяся структура (кристаллическая решетка) распространяется по всему объему тела, то образуется «одиночный кристалл» — монокристалл. Монокристаллы имеют форму правильных симметричных многоугольников. Но они редко достигают размеров в несколько сантиметров. Примерами монокристаллов могут служить драгоценные камни, исландский шпат (рис. 3), топаз (рис. 4).
В природе чаще встречаются беспорядочно сросшиеся между собой монокристаллы. Такие твердые тела называются поликристаллы. Примерами поликристаллов являются: каменная соль (рис. 5), кварц (рис. 6), сахар, лед, железо, медь.
Структурные особенности кристаллических тел
Кристаллические тела представляют собой материалы, структура которых обладает долгоразмерным порядком в расположении атомов или молекул. Это означает, что атомы или молекулы в кристаллическом теле упорядочены в регулярную решетку.
Основными характеристиками структуры кристаллических тел являются:
1. Цельность – все атомы или молекулы, составляющие кристаллическую решетку, образуют единую структурную единицу. Это означает, что взаимное расположение атомов или молекул внутри кристаллического тела одинаково на больших расстояниях.
2. Периодичность – структура кристалла повторяется в пространстве с периодичностью. Это значит, что кристалл можно представить как упорядоченную систему из однокубических нанометровых блоков, называемых элементарными ячейками.
3. Симметрия – у кристаллических тел часто наблюдается симметричная атомная или молекулярная решетка. Симметрия может быть отражательной, поворотной или поворотно-отражательной. Она определяет углы и длины связей между атомами или молекулами в кристаллической структуре.
4. Однозначность – структура кристаллического тела является однозначной и может быть полностью определена заданием значений индексов отражений в решетке Бравэ.
5. Дефекты – в кристаллической решетке могут наблюдаться дефекты, такие как примеси, вакансии, дислокации и т.д. Они влияют на механические, электрические и другие свойства кристалла.
Структурные особенности кристаллических тел определяют их физические свойства, такие как прозрачность, теплопроводность, оптические свойства и многое другое. Кристаллические материалы широко используются в различных отраслях науки и промышленности благодаря своим уникальным свойствам и возможностям.
Применение твердых аморфных
Твердые аморфные вещества обладают рядом уникальных свойств, которые делают их полезными в различных областях научных и промышленных приложений.
- Электроника: Твердые аморфные материалы могут использоваться в электронике для создания переносимых устройств, таких как смартфоны и планшеты. Их высокая электрическая проводимость и прочность делают их идеальными для изготовления микросхем и других электронных компонентов.
- Энергетика: Возможность твердых аморфных материалов сохранять большое количество энергии позволяет им использоваться в области хранения энергии. Они могут быть применены в аккумуляторах и суперконденсаторах, повышая эффективность энергетических систем.
- Медицина: Биосовместимость твердых аморфных материалов делает их применимыми в медицинской технологии. Они могут быть использованы для создания имплантатов и протезов, а также для доставки лекарственных препаратов в организм.
- Защита: Твердые аморфные материалы потенциально могут быть использованы в производстве брони и защитных покрытий. Их высокая прочность и стойкость к износу делают их эффективными при защите от воздействия внешних факторов.
- Нанотехнологии: Твердые аморфные материалы могут быть использованы в нанотехнологиях для создания наночастиц и наноструктур. Они обладают особыми магнитными, оптическими и электронными свойствами, что делает их привлекательными для исследования и разработки новых наноматериалов и устройств.
Применение твердых аморфных материалов в различных областях продолжает развиваться, и дополнительные исследования помогут раскрыть еще больше их потенциала.
Структура твердых кристаллических веществ
Твердые кристаллические вещества обладают определенной и упорядоченной структурой, которая отличает их от твердых аморфных веществ. Эта структура образуется благодаря регулярному повторению элементарных ячеек в трех измерениях.
Ячейка Бравэ
Основным строительным блоком структуры твердых кристаллических веществ является элементарная ячейка, которая повторяется в пространстве. Такую ячейку называют ячейкой Бравэ в честь французского физика Огюста Бравэ. Ячейка Бравэ может иметь различную форму, например, кубическую, гексагональную, тетрагональную и т.д.
Внутри ячейки Бравэ располагаются атомы или ионы, которые занимают определенные позиции в пространстве и образуют кристаллическую решетку.
Кристаллическая решетка
Кристаллическая решетка представляет собой упорядоченную сетку, состоящую из точек, каждая из которых соответствует позиции атома или иона в ячейке Бравэ. Расположение этих точек задается определенными правилами, причем симметрия и регулярность структуры являются характерными чертами кристаллических веществ.
Для описания кристаллической решетки используется так называемая элементарная ячейка, которая содержит как можно меньше точек и при этом сохраняет все симметричные свойства вещества.
| Тип решетки | Пример соединения |
|---|---|
| Кубическая | Соль (NaCl) |
| Гексагональная | Графит |
| Тетрагональная | Сцинтилляторы |
Кристаллические решетки характеризуются такими параметрами, как межатомное расстояние, координаты атомов, межплоскостное расстояние и др.
Знание структуры твердых кристаллических веществ позволяет проводить исследования и понимать их свойства и поведение в различных условиях.
Физические свойства
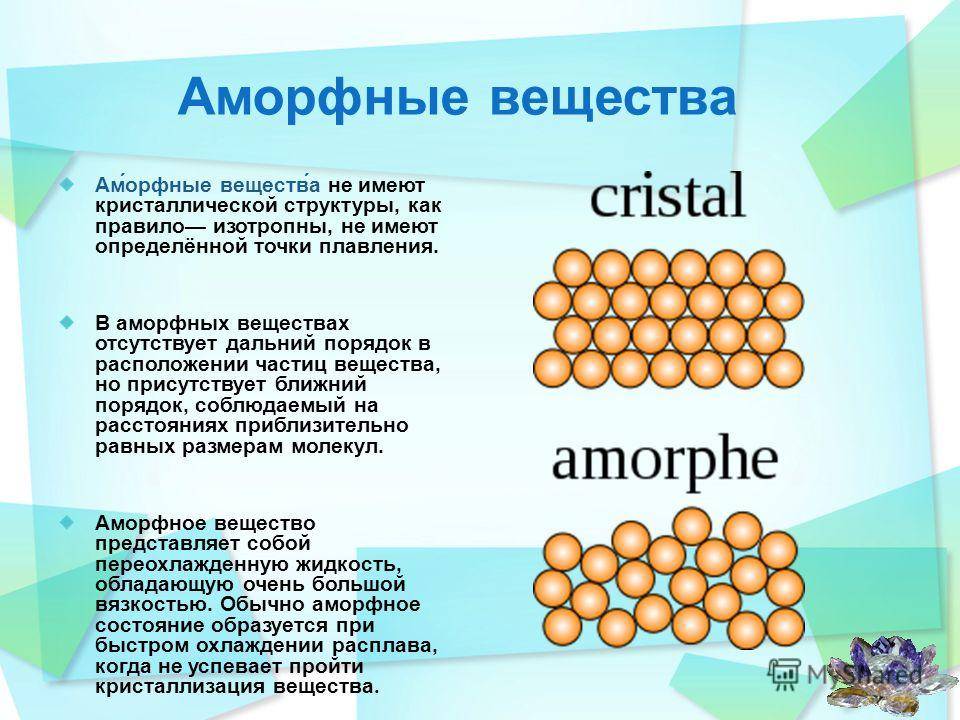
Аморфные тела, в отличие от кристаллических, не обладают долгоранжистой или периодической структурой, что определяет их основные физические свойства.
Одно из основных отличий между аморфными и кристаллическими телами заключается в их оптических свойствах. Аморфные материалы, будучи анизотропными, обладают случайным распределением индекса преломления в пространстве, что приводит к рассеянию света во всех направлениях. Кристаллические материалы, напротив, имеют предсказуемый индекс преломления, что позволяет им обладать определенной прозрачностью и возможностью преломления света.
Также аморфные материалы имеют более высокую плотность, чем кристаллические, что объясняется их более плотной упаковкой атомов в пространстве. Из-за этого аморфные материалы обладают повышенной твердостью и прочностью.
Еще одним важным физическим свойством аморфных тел является их высокая вязкость. В отличие от кристаллических материалов, аморфные имеют меньшую подвижность атомов, что приводит к более высокой вязкости
Это свойство может быть использовано, например, при производстве стекол и пленок, где важно иметь возможность легко формировать их в нужную форму и препятствовать их деформации в процессе использования
| Свойство | Аморфные тела | Кристаллические тела |
|---|---|---|
| Структура | Нерегулярная | Регулярная |
| Индекс преломления | Случайное распределение | Предсказуемый |
| Плотность | Более высокая | Более низкая |
| Твердость | Повышенная | Обычная |
| Вязкость | Высокая | Низкая |
Таким образом, физические свойства аморфных тел определяются их структурой, отличающейся от кристаллической, и включают оптические свойства, плотность, твердость и вязкость.
Твердость и ломкость
В кристаллических материалах атомы или молекулы располагаются в регулярной упорядоченной структуре, что придает им большую твердость. Кристаллические тела обычно являются твердыми и прочными. Они образуют кристаллы с определенными гранями и плоскостями.
В отличие от этого, аморфные тела не имеют регулярной кристаллической структуры, и их атомы или молекулы располагаются хаотично. Из-за этого аморфные материалы обладают меньшей твердостью. Они склонны к деформациям, царапинам и образованию сколов.
С другой стороны, аморфные тела обычно более прочные в направлении удаления атомов или молекул от плоскости структуры. Это связано с отсутствием сильных связей между атомами или молекулами в регулярной структуре кристаллических материалов. Поэтому, хотя аморфные материалы обладают меньшей твердостью, они могут быть более устойчивыми к разрушениям в определенных условиях.
Таким образом, твердость и ломкость являются важными свойствами материалов, отличающими кристаллические и аморфные тела. Кристаллические материалы обычно более твердые и менее склонные к деформациям, в то время как аморфные материалы обладают меньшей твердостью, но могут быть более прочными в некоторых случаях.
Проводимость
Аморфные тела имеют низкую проводимость по сравнению с кристаллическими структурами. Это связано с их хаотической и неупорядоченной структурой. В аморфных материалах электроны испытывают сложности при движении через материал из-за отсутствия определенных кристаллических направлений.
Кристаллические тела, напротив, имеют более высокую проводимость благодаря упорядоченной и регулярной структуре. Электроны могут свободно передвигаться по кристаллической решетке и эффективно проводить электрический ток.
Важно отметить, что проводимость аморфных и кристаллических материалов может зависеть от различных факторов, таких как тип и концентрация дефектов в структуре, температура и состав материала
Структура кристаллов
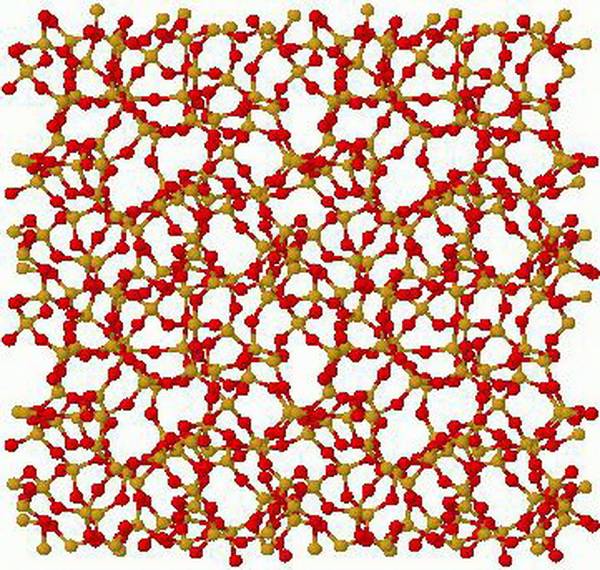 Рисунок 2. Структура кристаллов. Автор24 — интернет-биржа студенческих работ
Рисунок 2. Структура кристаллов. Автор24 — интернет-биржа студенческих работ
С кристаллической структурой веществ человек сталкивается постоянно в ежедневном режиме. Мы ходим зимой по снегу или льду, имеющим в своей основе чистую структуру кристалла. Она формируется из кристаллической воды. Многая пища состоит из кристалликов соли или сахара.
Такая многогранная натура твердых телах характеризуется несколькими схожими и постоянно повторяющимися элементами внутренней конструкции. Атомы и иные молекулярные связи располагаются в отдельных кристаллических решетках, при этом все выглядит предельно упорядоченно. Складывается система похожих многогранников. Таким образом, можно искусственным образом воспроизвести подобные молекулярные связи.
Упорядоченное расположение всех частиц в узлах кристаллической решетки придает правильную и красивую форму с симметричным расположением сторон и углов. Впервые такую структуру смогли показать и объяснить только 200 лет назад.
Для роста кристаллов необходимо создать определенные условия. Центр кристаллизации становится своеобразной точкой отсчета будущего каркаса вещества. Его можно создать искусственным или естественным способом. Для этого в прозрачном растворе наблюдают за движением ионов или молекул. Они ведут себя достаточно непредсказуемым образом и постоянно сталкиваются, при этом идет формирование новых протосвязей – зародышей будущего кристаллического твердого тела. При повторных взаимодействиях можно увидеть, что приобретаются формы структуры мельчайшего кристаллика, который станет элементом ячейки тела. Под скоплением частиц происходит постепенный рост решетки, при этом появляется тот самый центр кристаллизации. Его основой могут быть самые разнообразные вещества, которые содержатся и плавают в сосуде. В процессе роста появляются дополнительные связи и происходит превращение в большое твердое тело с кристаллической основой.
Применение
Аморфные тела и кристаллические материалы имеют различные свойства и структуру, что позволяет им находить применение в различных областях.
- Аморфные тела используются для создания быстрых стекол, которые обладают высокой скоростью охлаждения и хорошей аморфностью. Эти стекла находят применение в производстве оптических волокон, лазеров, оправ для очков и другой оптической техники.
- Кристаллические материалы применяются для создания полупроводниковых приборов, таких как транзисторы и диоды. Кристаллическая структура позволяет достичь контроля над электрическими свойствами материала.
- Аморфные тела также применяются в фармацевтической и пищевой промышленности для создания лекарственных форм и пищевых добавок. Благодаря своей аморфной структуре, они могут обладать улучшенной стабильностью и растворимостью.
- Кристаллические материалы используются в ювелирной промышленности для создания драгоценных камней и украшений. Их превосходная прозрачность и блеск делают их особенно ценными.
- Аморфные тела применяются в производстве электронных устройств, таких как жидкокристаллические дисплеи и плоские панели. Благодаря своей аморфной структуре, они обладают высокой электрической проводимостью и могут быть использованы в различных электронных приборах.
Таким образом, аморфные тела и кристаллические материалы играют важную роль в современной науке и технологии, применяясь в различных областях от оптики и электроники до фармацевтики и ювелирного искусства.
Использование аморфных тел
Аморфные тела обладают рядом уникальных свойств, которые находят применение в различных областях науки и техники.
Одним из основных преимуществ аморфных тел является их высокая пластичность. Благодаря отсутствию регулярной кристаллической структуры, аморфные материалы могут подвергаться сильным деформациям без разрушения. Это позволяет использовать их в производстве гибких и изгибаемых изделий, таких как гибкие электронные устройства или солнечные батареи в тонких пленках.
Также аморфные тела обладают высокой прозрачностью для оптического излучения. Это делает их незаменимыми для создания оптических элементов, например, в оптических волокнах или солнечных батареях. Аморфные материалы, такие как аморфный кремний или аморфный графит, обладают большими возможностями в области фотоэлектрического преобразования энергии.
Кроме того, аморфные тела обладают высокой химической инертностью. Это означает, что они не реагируют с различными веществами и не подвержены коррозии. Благодаря этим свойствам, аморфные материалы широко используются для создания покрытий и защитных слоев на различных поверхностях, таких как корпусы электроники или поверхность стекла.
Таким образом, использование аморфных тел позволяет создавать инновационные и устойчивые по своим свойствам материалы, которые находят применение в различных областях науки, техники и промышленности.
Особые свойства твердых тел
- Анизотропия – одно из свойств твердого вещества, которое заключается в зависимости физических свойств от направления в кристалле.
- Изотропия – отсутствие зависимости свойства тела от направления
- Полиформизм – особое свойство, которое заключается в способности твёрдых тел находиться в состоянии с различной кристаллической решёткой. Свойство присуще только твердому агрегатному состоянию веществ.
Молекулы и атомы тел типа аморфные поддаются колебаниям, однако незначительным по сравнению с жидкостью, поэтому по внутренним свойствам их можно приравнять к кристаллическим.
Их атомы не находятся в постоянном процессе перестраивания из одного положения в другое, поэтому их состояние равновесия характеризуется как неменяющееся. Аморфные тела в состоянии низкой температуры отвечают свойствам твердых тел. При повышении температуры – меняются связи на молекулярном уровне, а тела начинают напоминать по своим свойствам жидкость.
Аморфные тела имеют одновременно схожесть и с кристаллическими, и с твердыми телами, и с жидкими. Из частицы находятся в определенном порядке, что позволяет создавать материалы, вещества, предметы с заданными и ожидаемыми свойствами. Управляемые свойства твердых тел физика рассматривает как одно из самых основных направлений практически ориентированного изучения того, какими общими свойствами обладают твердые тела и как этими свойствами управлять.
Не нашли ответ?
Просто напиши,с чем тебе нужна помощь
Мне нужна помощь
Кристаллические дефекты и их влияние на свойства вещества
Основные типы кристаллических дефектов включают дислокации, вакансии, внеплоскостные дефекты и дефекты решетки. Дислокации представляют собой дефекты, связанные с наличием дополнительной плоскости атомов в кристаллической решетке. Эти дефекты могут перемещаться внутри кристалла и играть ключевую роль в пластической деформации материала.
Вакансии являются атомными пропусками в решетке. Они могут возникать в результате тепловых флуктуаций или под воздействием внешних факторов. Вакансии изменяют плотность атомов в кристаллической структуре и могут приводить к изменению физических свойств вещества, таких как электропроводность и теплопроводность.
Внеплоскостные дефекты связаны с наличием атомов или молекул вне основной кристаллической решетки. Эти дефекты могут возникать в результате внешнего воздействия или неправильной структуры материала. Внеплоскостные дефекты могут влиять на механические свойства материала, такие как твердость и прочность.
Дефекты решетки возникают в результате нарушения геометрической структуры кристаллической решетки. Это могут быть сдвиги, искривления или разрывы кристаллической структуры. Дефекты решетки также могут влиять на электрические, оптические и магнитные свойства материала.
| Тип дефекта | Описание | Влияние на свойства вещества |
|---|---|---|
| Дислокации | Дополнительные плоскости атомов в решетке | Влияние на пластическую деформацию и механическую прочность |
| Вакансии | Атомные пропуски в решетке | Изменение электропроводности и теплопроводности |
| Внеплоскостные дефекты | Атомы или молекулы вне основной решетки | Влияние на механические свойства, такие как твердость и прочность |
| Дефекты решетки | Нарушение геометрической структуры решетки | Влияние на электрические, оптические и магнитные свойства |
Кристаллические дефекты могут быть как полезными, так и нежелательными. С одной стороны, они могут улучшать свойства вещества, например, делать его более прочным или проводящим. С другой стороны, дефекты могут приводить к ухудшению свойств, например, вызывать ломкость или низкую электропроводность. Понимание дефектов и их влияния на свойства вещества позволяет разрабатывать новые материалы с определенными свойствами и улучшать уже существующие.
Строение и свойства твердых тел.
- В каких агрегатных состояниях может находиться вещество?
- Какие тела называют аморфными?
- Чем отличаются монокристаллы от поликристаллов?
- Что вы понимаете под изотропией и анизотропией?
- Как ведут себя молекулы в твердых телах?
Молекулярное строение твердых тел
Твердое тело имеет собственную форму, не растекается по объему и не принимает его форму. На микроскопическом уровне атомы прикрепляются друг к другу химическими связями, и их положение друг относительно друга фиксировано. При этом они могут образовывать как жесткие упорядоченные структуры — кристаллические решетки.
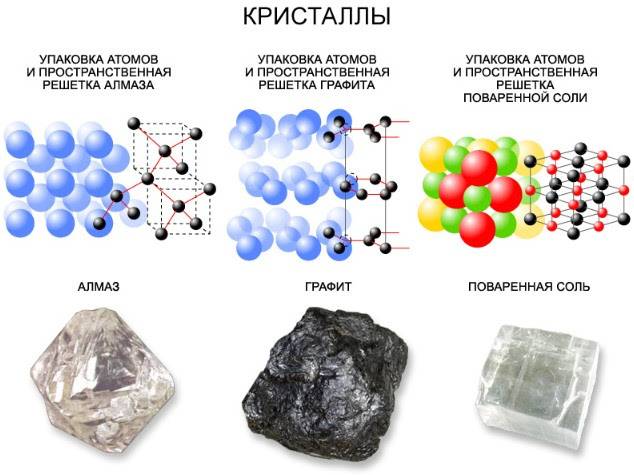
Кристаллическое тело может состоять из одного кристалла (монокристалл). Может состоять из многих “сросшихся” кристаллов (поликристаллы).
Монокристалл Поликристалл
Монокристаллы обладают анизотропией, поликристаллы изотропны. Анизотропия – различие свойств по разным направлениям. Прежде всего, бросается в глаза различная механическая прочность кристаллов по разным направлениям. Например, кусок слюды легко расслаивается в одном из направлений на тонкие пластинки, но разорвать его в направлении, перпендикулярном пластинкам, гораздо труднее. Так же легко расслаивается в одном направлении кристалл графита. Когда вы пишете карандашом, такое расслоение происходит непрерывно и тонкие слои графита остаются на бумаге. Многие кристаллы по-разному проводят теплоту и электрический ток в различных направлениях. От направления зависят и оптические свойства кристаллов. Так, кристалл алмаза по-разному преломляет свет в зависимости от направления падающих на него лучей.
Молекулы (ионы, атомы), образующие кристаллическую решетку, колеблются около положения узла, отклоняясь на малые, по сравнению с расстоянием между узлами, расстояния. Чем выше температура тела, тем больше размах колебаний молекул. Кинетическая энергия молекул значительно выше потенциальной энергии их взаимодействия.
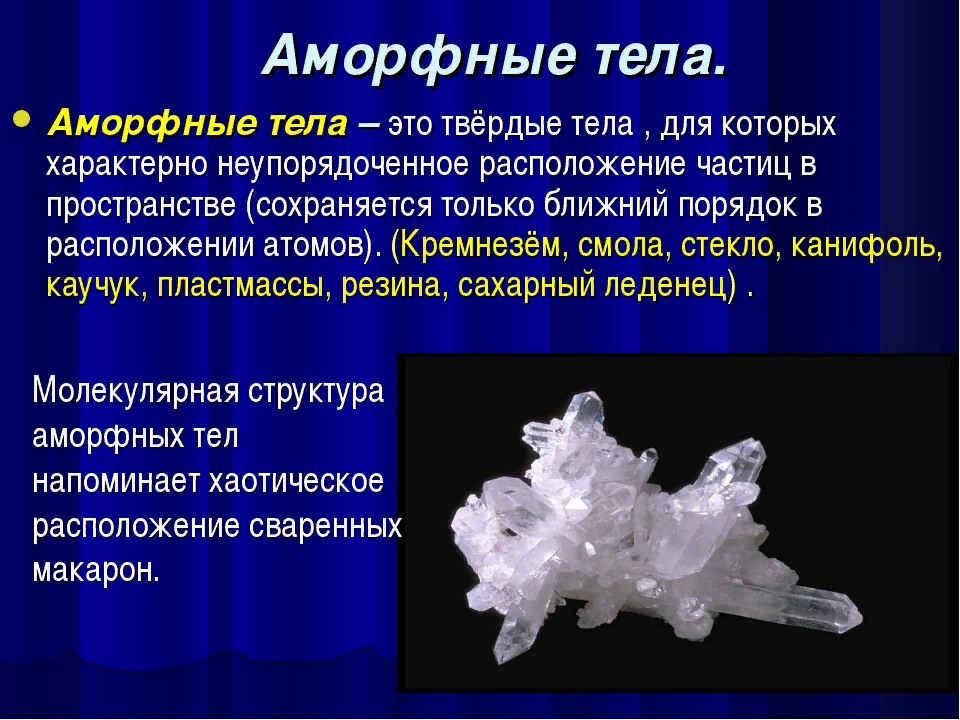
Аморфные тела
Если связанные атомы образуют беспорядочные нагромождения, получим аморфное тело (именно такова структура полимеров, которые похожи на перепутанные и слипшиеся макароны в миске). К аморфным телам относятся стекло, смола, канифоль, сахарный леденец и др.
Следует иметь в виду, что в ряде случаев одно и то же вещество в зависимости от условий его получения может находиться как в кристаллическом, так и в аморфном состоянии. Так как аморфные тела могут самопроизвольно переходить в кристаллическое состояние, следует, что кристаллическая форма вещества более устойчива, чем аморфная.
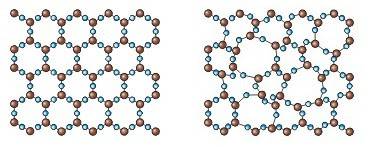
Молекулы кварца: а) кристаллического, б) аморфного.
С точки зрения молекулярного строения аморфные тела следует отнести не к твердым телам – кристаллам, а к жидкостям с очень большой вязкостью.
Все аморфные тела изотропные, т.е. их физические свойства одинаковы по всем направлениям.
Молекулы аморфных тел движутся так, как движутся молекулы жидкостей, но их подвижность очень мала.
Жидкие кристаллы
Это фазовое состояние, в которое переходят некоторые вещества при определенных условиях (температура, давление, концентрация в растворе). Жидкие кристаллы обладают одновременно свойствами как жидкостей (текучесть), так и кристаллов (анизотропия).
По структуре представляют собой вязкие жидкости, состоящие из молекул вытянутой или дискообразной формы, определённым образом упорядоченных во всем объёме этой жидкости.
Модель жидкого кристалла
Кристаллические тела
Твердые тела, в которых молекулы и атомы расположены упорядоченно и образуют периодически повторяющуюся структуру, называются кристаллами. Физические свойства кристаллов (упругие, механические, тепловые, электрические, магнитные, оптические) в разных направлениях неодинаковы. Такое свойство называется анизотропностью. Анизотропия кристаллов объясняется тем, что при упорядоченном расположении частиц расстояния между ними и силы взаимодействия (притяжения и отталкивания) оказываются неодинаковыми в разных направлениях.
Различают кристаллические тела двух видов: монокристаллы и поликристаллы. Главным признаком монокристаллов является повторяющееся внутреннее строение (структура) во всем объеме тела.
Поликристалл — это совокупность (набор) сросшихся друг с другом, хаотически ориентированных, небольших кристаллов. Каждый маленький кристалл обладает свойствами анизотропии, но их совокупность — поликристалл — изотропен.
Рис. 2. Монокристаллы и поликристаллы.
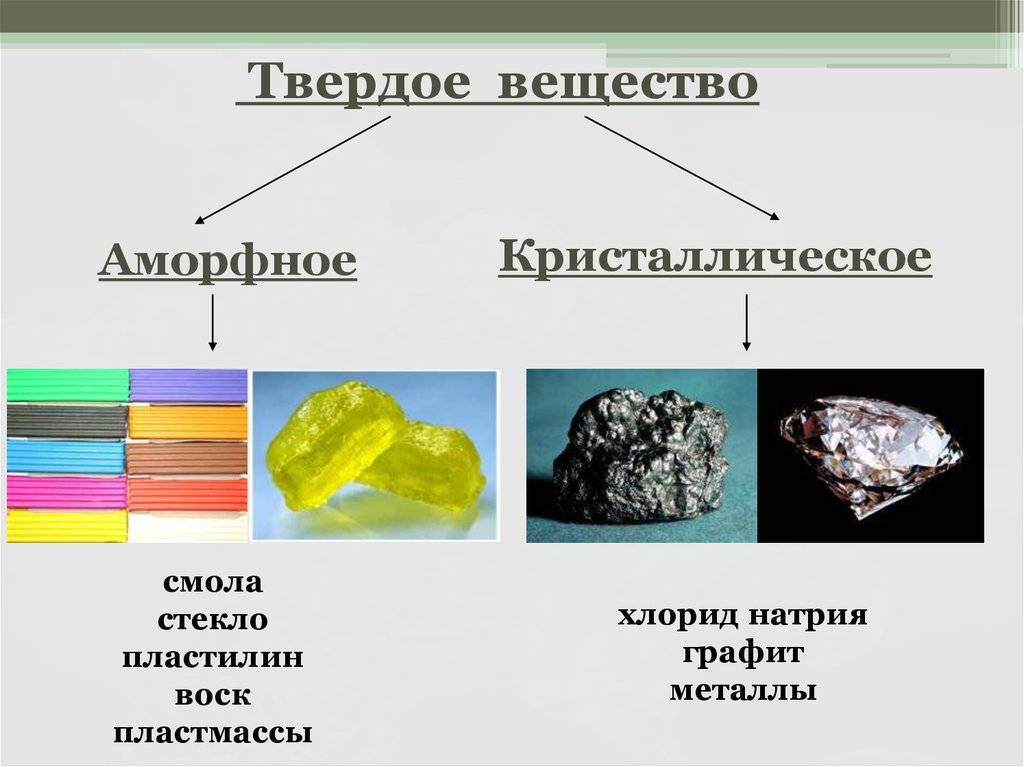
Часто встречаются кристаллические тела одинаковые по своему химическому составу, но обладающие очень разные физические свойства. Самый известный пример — это углерод, имеющий две модификации: графит и алмаз. Разное строение кристаллических решеток является причиной того, что алмаз имеет рекордные показатели твердости, а графит из-за его мягкости используется в качестве грифелей для карандашей.
Рис. 3. Графит и алмаз.
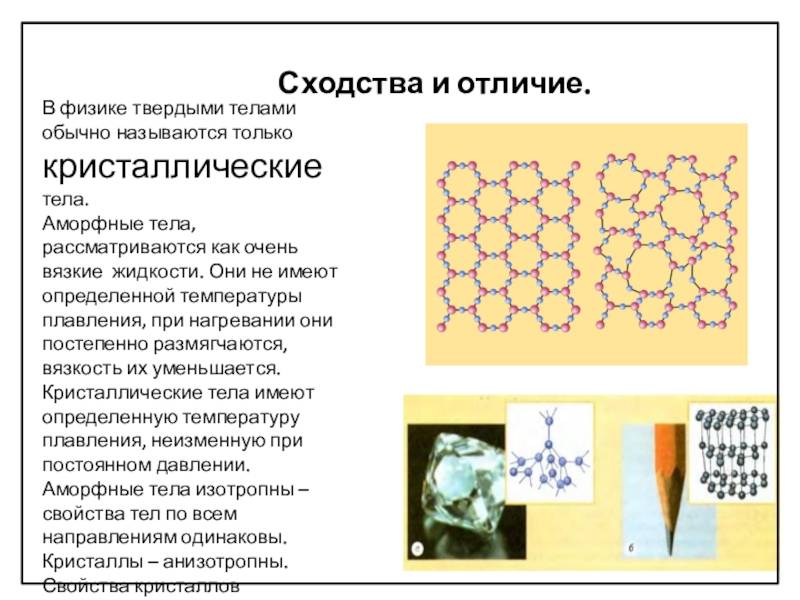
Что мы узнали?
Итак, мы узнали, что кристаллические и аморфные тела кроме общих признаков, которые относят их к твердым телам, имеют совершенно разные физические свойства. Аморфные тела обладают изотропными свойствами, а для кристаллов характерна анизотропия физических параметров. Кристаллические тела делятся на монокристаллы и поликристаллы.
/5
Вопрос 1 из 5