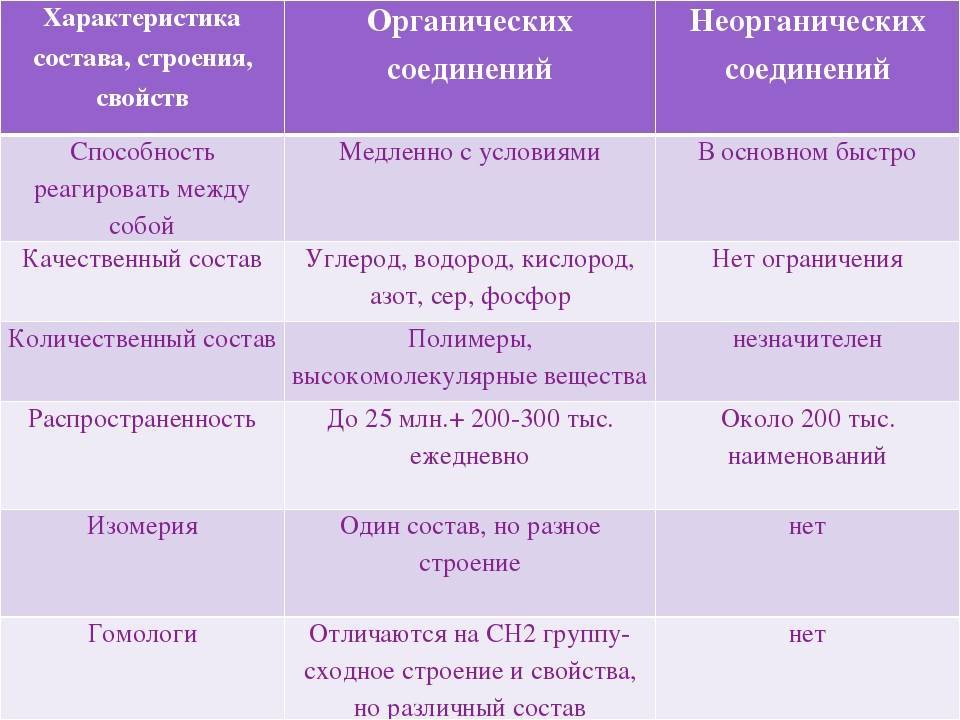
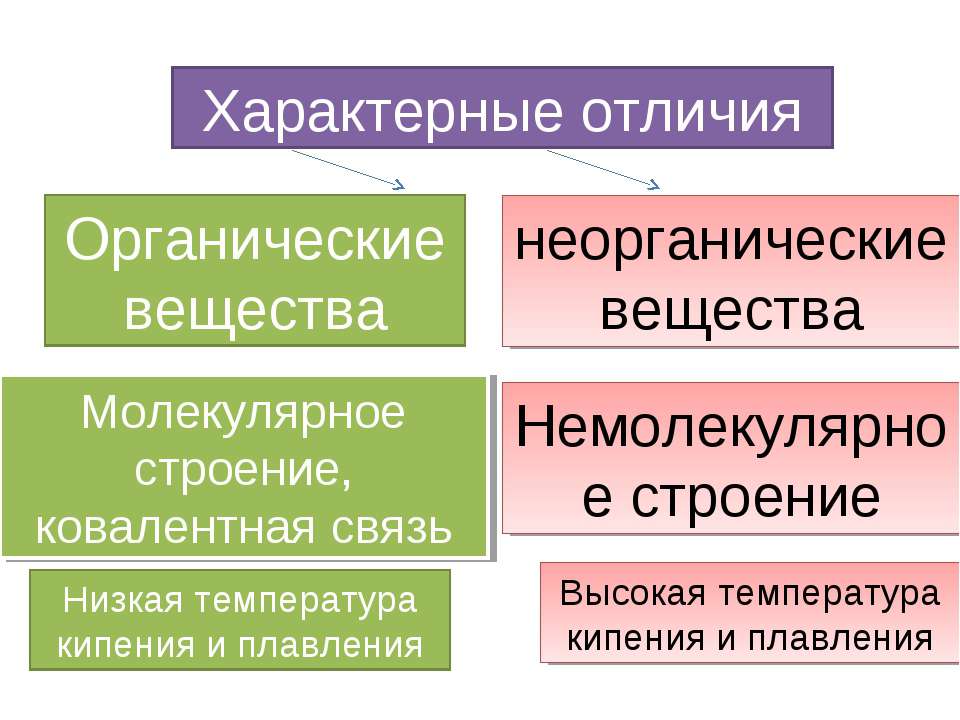
Содержание основных элементов питания в навозе
В состав навоза входят компоненты, которые обеспечивают питание растениям, улучшают физико-химические свойства почвы, ее структуру. Являясь источником органики, навоз при ферментации формирует гумусовые соединения, повышающие естественное плодородие почвы.
Навоз в любых состояниях (свежий, полуперепревший, перегной) – это источник макро– и микроэлементов, таких как азот, фосфор, калий, кальций, кремний, сера, хлор, магний, бор, марганец, кобальт, медь, цинк, молибден. Активные микроорганизмы навоза являются главным источником энергии для почвенной микрофлоры.
Все виды навоза отличаются щелочными свойствами, показатель щелочности доходит до рН=8-9 единиц. У коровьего навоза он равен 8,1, у конского – 7,8, у свиного – 7,9 единиц. Естественно, что их внесение ощелачивает почву, снижая кислотность. Содержание основных элементов питания представлены в усредненных показателях таблицы 1.
5. FAQ
5.1. Являются ли все органические соединения безопасными для потребления?
Нет, не все органические соединения безопасны для потребления. Например, некоторые органические соединения могут быть токсичными или вызывать аллергические реакции
Поэтому важно следовать рекомендациям и указаниям по использованию и потреблению продуктов, содержащих органические соединения
5.2. Какие неорганические соединения могут быть опасными для здоровья?
Некоторые неорганические соединения, такие как свинец, ртуть и асбест, могут быть опасными для здоровья. Они могут накапливаться в организме и вызывать различные заболевания
Поэтому важно соблюдать меры предосторожности при работе с такими веществами и следовать рекомендациям по безопасности
5.3. Какие преимущества органического сельского хозяйства перед неорганическим?
Органическое сельское хозяйство имеет ряд преимуществ перед неорганическим. Оно способствует сохранению плодородия почвы, повышению качества продуктов питания, снижению использования химических удобрений и пестицидов, а также улучшению условий жизни животных. Органическое сельское хозяйство также способствует сохранению биоразнообразия и снижению негативного воздействия на окружающую среду.
5.4. Можно ли преобразовать органические соединения в неорганические и наоборот?
Да, в некоторых случаях органические соединения могут быть преобразованы в неорганические и наоборот. Например, при сжигании органических материалов, таких как дерево или уголь, происходит окисление углерода до неорганического углекислого газа. Также, некоторые неорганические соединения могут быть использованы в химических реакциях для получения органических соединений.
5.5
Важно ли различать органическое и неорганическое в повседневной жизни?. Различие между органическим и неорганическим может быть важно в определенных ситуациях
Например, при выборе продуктов питания, мы можем предпочесть органические продукты, чтобы избежать употребления вредных химических веществ. Также, различие между органическим и неорганическим может быть важным при выборе материалов для строительства или при использовании химических веществ в быту или на работе
Различие между органическим и неорганическим может быть важно в определенных ситуациях. Например, при выборе продуктов питания, мы можем предпочесть органические продукты, чтобы избежать употребления вредных химических веществ
Также, различие между органическим и неорганическим может быть важным при выборе материалов для строительства или при использовании химических веществ в быту или на работе.
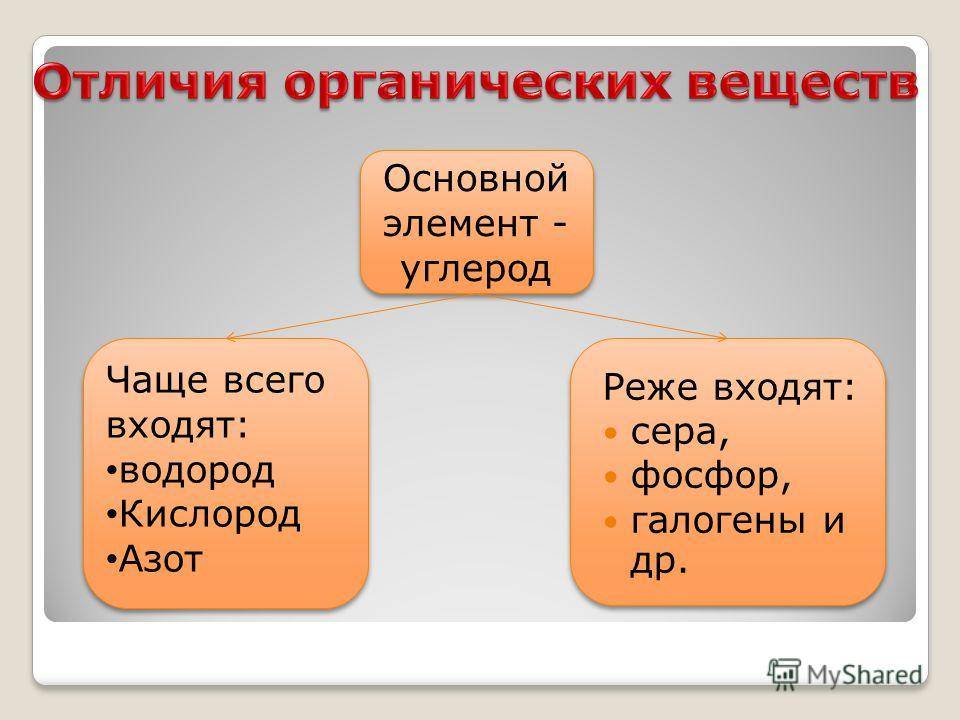
Особенности органических веществ
Органические вещества — это химические соединения, которые содержат в своей структуре углеродные атомы. Углерод является основным элементом, который отличает органические вещества от неорганических. Органические вещества обладают рядом особенностей, которые делают их уникальными в мире химии.
1. Сложность структуры и разнообразие соединений.
Органические вещества могут иметь очень сложную структуру. В их составе могут присутствовать разные типы связей между атомами углерода и другими элементами. Это позволяет создавать огромное количество разнообразных соединений, начиная от простейших углеводородов и заканчивая сложными белками и ДНК.
2. Изотопы и аллотропия.
Органические вещества могут существовать в различных изотопных формах, то есть иметь различное количество нейтронов в атомном ядре. Изотопы органических веществ могут обладать разными свойствами и использоваться в различных областях науки и технологий.
Также органические вещества могут образовывать разные аллотропные формы. Например, углерод может существовать в виде алмаза, графита, фуллерена и других форм. Каждая из этих форм обладает своими уникальными свойствами и применениями.
3. Связанность соединений.
Органические вещества обладают высокой связанностью между атомами. Это обусловлено наличием сильных ковалентных связей, которые образуются между углеродом и другими атомами. Благодаря этой связанности органические вещества имеют высокую устойчивость и стабильность.
4. Биологическая значимость.
Органические вещества являются основой для жизни на Земле. Большинство органических соединений присутствуют в живых организмах и выполняют различные функции. От них зависят жизненно важные процессы, такие как обмен веществ, рост, размножение и др.
5
Важность для промышленности и науки
Органические вещества имеют огромное значение в промышленности и науке. Они используются для производства пластмасс, лекарств, синтетических волокон, красителей, косметики и многих других продуктов. Органическая химия является одной из основных областей химии и позволяет синтезировать и изучать новые вещества и материалы.
6. Влияние окружающей среды.
Органические вещества могут быть очень чувствительными к воздействию окружающей среды. Некоторые органические соединения могут разлагаться при высоких температурах, взаимодействовать с кислородом или другими реагентами, быть токсичными для живых организмов и окружающей среды
Поэтому важно соблюдать меры предосторожности при работе с органическими веществами
Органические вещества играют огромную роль в нашей жизни и являются основой многих процессов и технологий. Изучение свойств и химических реакций органических веществ позволяет расширить наши знания о мире и создать новые материалы и продукты, которые улучшают нашу жизнь.
Применение полуперепревшего навоза
Полуперепревший навоз менее концентрированный и его можно использовать непосредственно в подкормках или в качестве мульчи.
Для подкормок готовят раствор в концентрации: одну часть удобрения на 10 частей воды. Размешивают и вносят под садово-ягодные культуры.
Деревья поливают по наружному диаметру кроны на разрыхленную почву или в борозды, нарезанные в 1-2 ряда вокруг кроны.
Под кустарники вносят подкормку отступив 15-20 см от кустов.
Под овощные культуры в борозды междурядий (если они широкие) или в борозды, нарезанные вдоль грядки.
Под корень растений раствор полуперепревшего коровяка лить нельзя.
Подкормку закрывают почвой, если необходимо, поливают и мульчируют.
Полуперепревшая масса является хорошим удобрением для капусты, тыквенных, шпината. При таком удобрении эти культуры будут великолепными предшественниками для корнеплодов, перца сладкого, томатов, баклажанов.
Применение органических веществ
Органические вещества – это класс химических соединений, объединяющий все вещества, в состав которых входит углерод.
Предельные (насыщенные) углеводороды, атомами водорода: СН4 – метан (основа природного газа), С2Н6 – этан, С3Н8 – пропан, С8Н18 – октан (основа бензина).
Широко распространено применение данной группы органических соединений в химической промышленности (для производства пластмасс, синтетических волокон и т.д.) и медицине.
Соединения служат исходными веществами для получения ряда готовых продуктов:
- растворителей (спиртов, дихлорэтана, эфира);
- полимеров (полиэтилена, поливинилхлорида, полиизобутилена);
Этилен (Н2С=С Н2) используется для получения, тефлона, этилового спирта, уксусного альдегида, галогенопроизводных и многих других органических соединений.
Алкены применяются и для ускорения процесс созревания фруктов.
Алкины (ацетиленовые углеводороды)
Ацетилен – необходим в качестве исходного продукта в органическом синтезе при производстве:
- полимеров (каучука, поливинилхлорида и др.);
- растворителей (1,1,2,2-тетрахлорэтана , 1,1,2-трихлорэтена);
- уксусной кислоты.
Температура пламени вещества достигает 3150°С, что нашло свое применение при резке металла и в сварке.
Алкоголи – производные углеводородов, в которых один или несколько атомов водорода замещены на гидроксильную группу ОН.
Метанол (СН3ОН) –применяется в производстве муравьиной кислоты и формальдегида. Рассматривается как вариант для применения в качестве моторного топлива.
Этанол (С2Н5ОН)- востребован в виде исходного соединения для получения уксусной кислоты, сложных эфиров, карбоновых кислот. Вещество служит основой производства спиртосодержащей продукции и антисептических средств.
Этиленгликоль – компонент необходимый в производстве пластмасс, антифризов, органическом синтезе.
Глицерин – незаменим в разных отраслях промышленности, в том числе текстильной, пищевой, фармакологии.
Основное использование соединений приходится на химическую промышленность, медицину (производство синтетических смол, красителей, антисептиков, взрывчатых веществ и т.д.).
Метаналь – используется при получении фенолформальдегидных и карбамидных смол, синтезе лекарственных средств, как дезинфицирующее средство.
Этаналь — нашел свое применение в органическом синтезе.
Карбоновые кислоты
Соединения, карбоксильной группы –СООН.
Муравьиная кислота (НСООН) –применяется в фармацевтической и пищевой промышленности. Уксусная кислота (СН3СООН) — востребована для производства искусственных волокон на основе целлюлозы и в пищевой промышленности.
Бензойная кислота (С6Н5СООН) – незаменима в фармацевтике для синтеза душистых веществ и красителей, а также в качестве консерванта для пищевых продуктов.
Сложные эфиры
Применяются в пищевой и парфюмерной отраслях в качестве отдушек. А также обеспечивают эластичность и пластичность пластмасс и резины.
Также широко распространено в пищевой промышленности, медицине применение глюкозы, аминов, аминокислот. Целлюлоза основной компонент при изготовлении бумаги, пленок, искусственных волокон и т.д.
Много соединений еще не изучено до конца, и возможно, благодаря науке человек сможет заменить натуральные продукты на искусственные, органических соединений природного происхождения применяется все меньше.
Доклад про святую екатерину
Социалистическая правовая семья доклад
Умения и навыки доклад
Доклад военнослужащего начальнику о происшествии
- Доклад на тему гироскопический датчик
Во всём нужен порядок
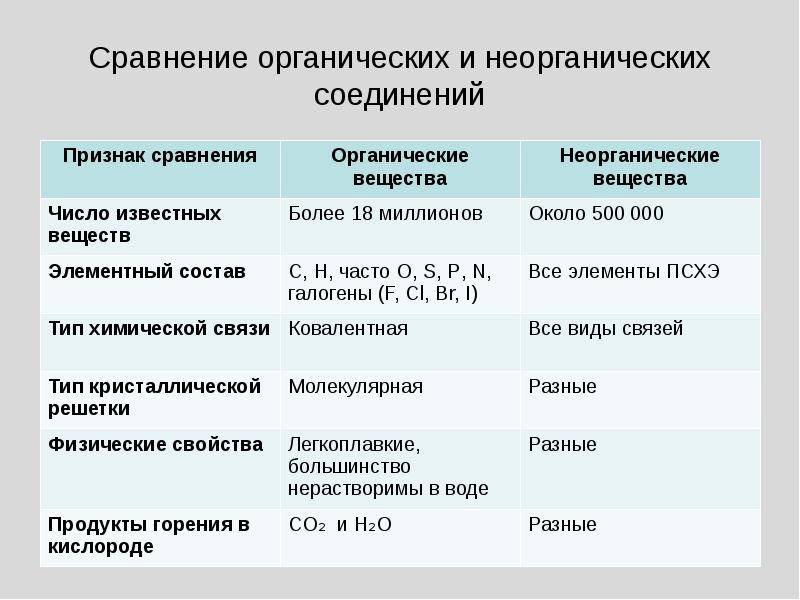
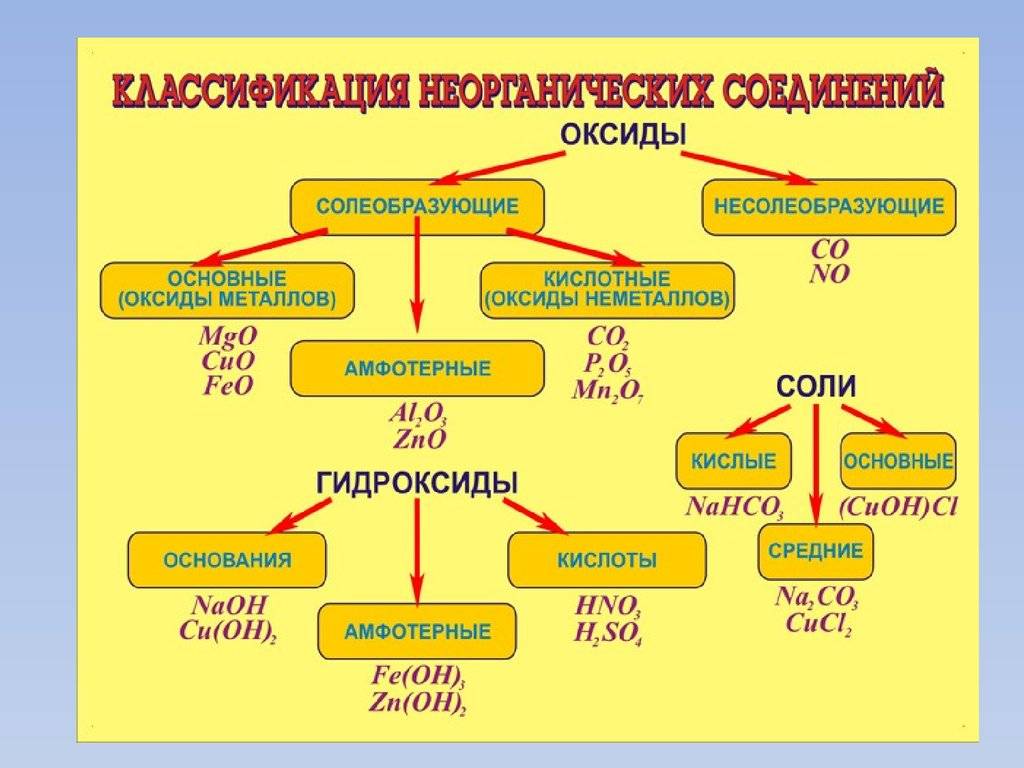
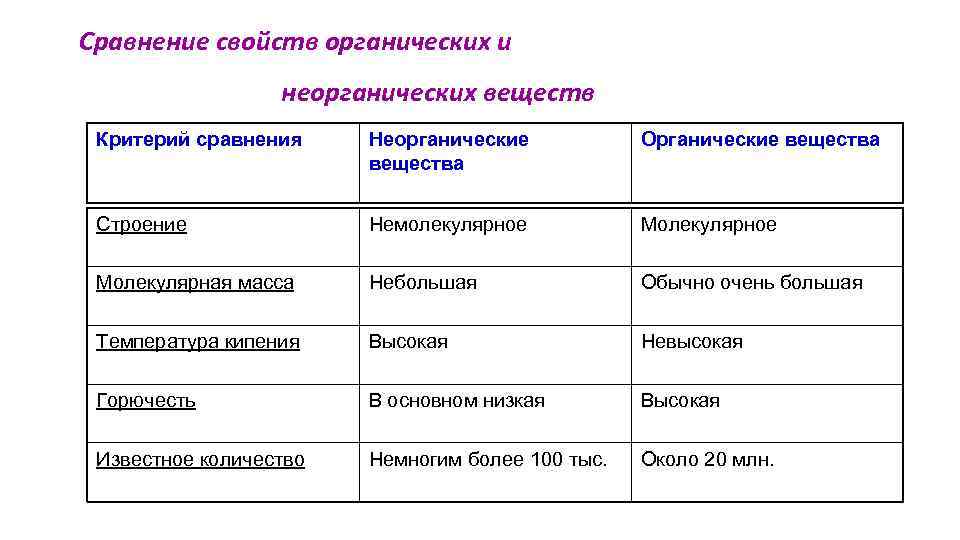
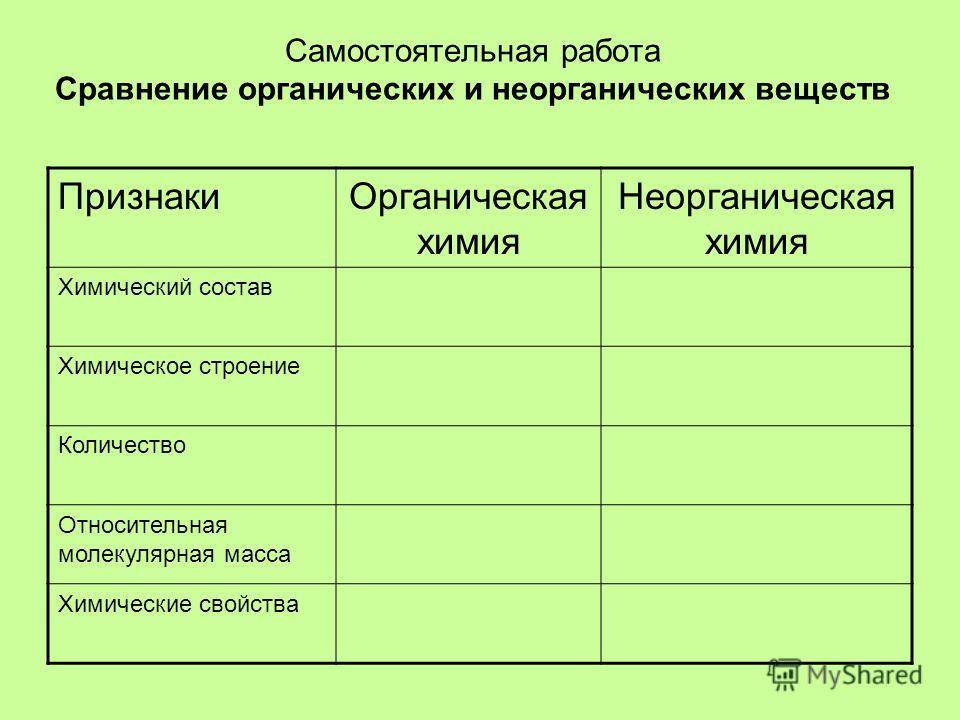
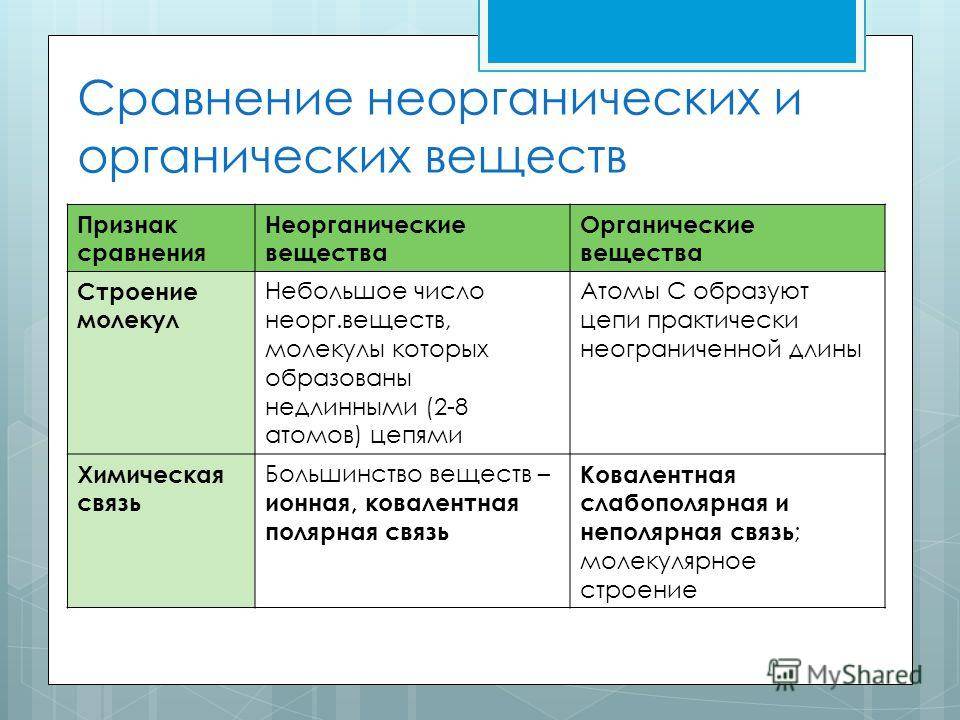
Неорганические вещества обычно подразделяют на простые и сложные. Первые состоят из одинаковых атомов. Атомы разных элементов образуют сложные вещества: оксиды, гидроксиды, кислоты, соли. Возможны и другие подходы. Например, классифицировать на основе одного из элементов: соединения железа, соединения хлора.
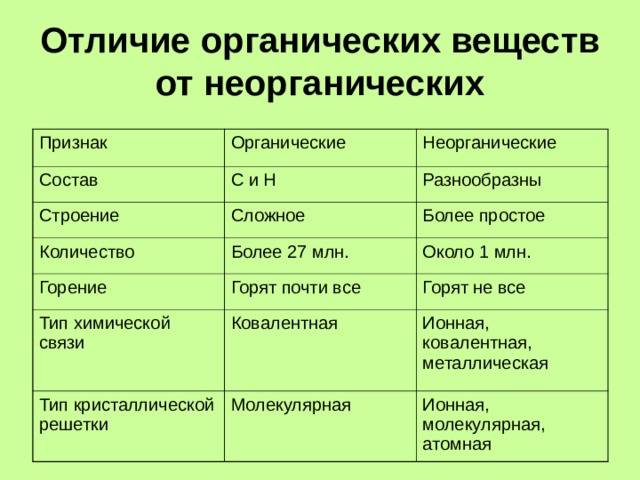
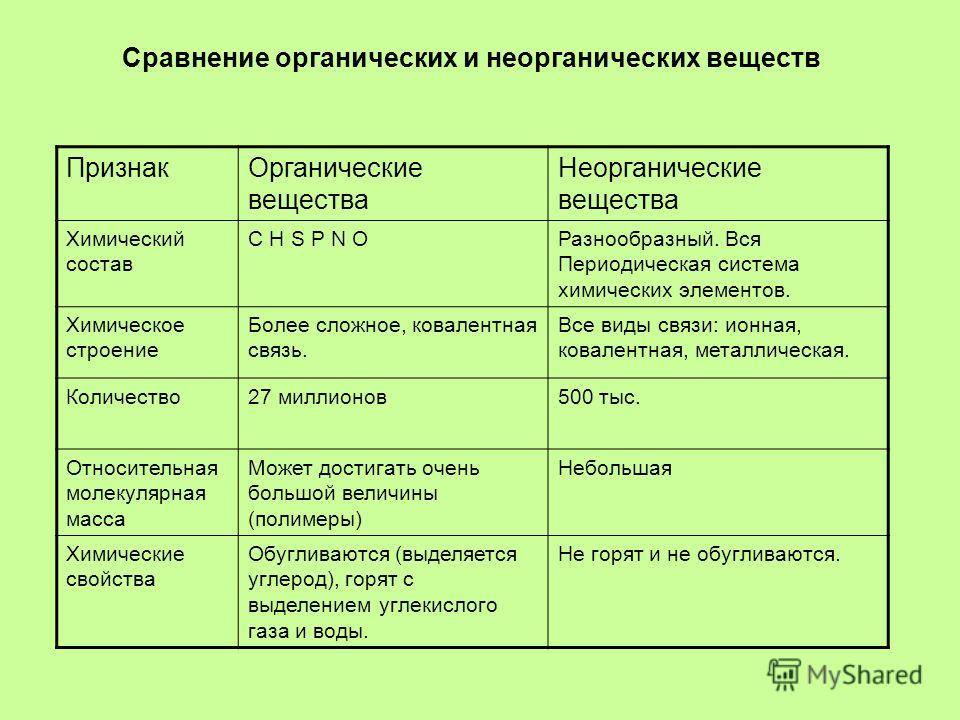
У органических веществ классов побольше. По составу и строению их обычно подразделяют на белки, аминокислоты, липиды, жирные кислоты, углеводы, нуклеиновые кислоты. На базе их биологического действия органические соединения можно группировать в алкалоиды, ферменты, витамины, гормоны, нейромедиаторы и др.
Классификация предполагает и «называние». Само собой, разные соединения должны всегда носить разные имена и при этом желательно, чтобы по имени можно было судить о самом веществе. Но когда речь идёт о миллионах разных названий… Как вам такое: (6E,13E)-18-бромо-12-бутил-11-хлоро-4,8-диэтил-5-гидрокси-15-метокситрикоза-6,13-диен-19-ин-3,9-дион? Оно составлено по всем официальным правилам органической химии. Ясно, что самые длинные слова надо искать именно в мире органики. В русском языке рекордсменом считают словечко «тетрагидропиранилциклопентилтетрагидропиридопиридиновое» ( 55 букв!). Но это далеко не предел. В наших мышцах есть белок титин, полное химическое название которого в английском варианте состоит из 189 819 букв и произносится примерно три с половиной часа. Надеемся, вы не обидитесь, если мы публиковать его здесь не будем.
Ясно, что самые длинные слова надо искать именно в мире органики. В русском языке рекордсменом считают словечко «тетрагидропиранилциклопентилтетрагидропиридопиридиновое» ( 55 букв!). Но это далеко не предел. В наших мышцах есть белок титин, полное химическое название которого в английском варианте состоит из 189 819 букв и произносится примерно три с половиной часа. Надеемся, вы не обидитесь, если мы публиковать его здесь не будем.
Неорганические вещества
Неорганические вещества могут быть найдены в природе, созданы и использованы человеком как строительные материалы, катализаторы, добавки в пищу и многое другое.
Неорганические вещества имеют разнообразные свойства, такие как проводимость тепла и электричества, прочность, растворимость в воде и других растворителях, а также способность образовывать кристаллическую структуру.
Многие неорганические вещества имеют важное практическое применение. Например, металлы широко используются в производстве различных изделий и машин
Соли, такие как хлорид натрия и сернистый кислород, используются в медицине и пищевой промышленности. Керамика и стекло, также являющиеся неорганическими веществами, применяются в строительстве и производстве посуды.
Важно отметить, что неорганические вещества могут взаимодействовать с органическими веществами, что ведет к образованию различных химических соединений
Определение и свойства
Органические вещества обладают следующими характеристиками:
- Образуют ковалентные связи. Органические соединения содержат один или несколько углеродных атомов, которые связаны с другими атомами посредством ковалентных связей.
- Обладают высокой температурой кипения и плавления. Большинство органических веществ обладают более низкими температурами кипения и плавления, чем неорганические вещества.
- Могут быть сжигаемыми. Органические вещества могут сгореть при наличии кислорода, и в результате возникают два продукта — углекислый газ и вода.
- Могут образовывать растворы. Органические вещества могут растворяться в различных растворителях, таких как вода, спирт и другие органические соединения.
- Обладают способностью образовывать многочисленные соединения. Органические вещества могут образовывать огромное разнообразие соединений, благодаря наличию углерода и его способности образовывать ковалентные связи.
Неорганические вещества, в отличие от органических, не содержат углерода в их структуре. Они могут быть как живыми, так и неживыми веществами. Примеры неорганических веществ включают минералы, металлы, соли, воду и газы, такие как кислород и азот.
Неорганические вещества также имеют свои характеристики:
- Могут образовывать ионные связи. Соединения, состоящие из неорганических веществ, обычно образуются путем обмена электронами и формирования ионных связей.
- Могут обладать высокой температурой кипения и плавления. Некоторые неорганические вещества обладают очень высокой температурой кипения и плавления, например, металлы.
- Могут образовывать растворы. Некоторые неорганические вещества могут растворяться в воде или других растворителях, образуя ионы в растворе.
- Могут обладать электропроводностью. Некоторые неорганические вещества, такие как соли или кислоты, могут проводить электрический ток в растворе или в твердом состоянии.
Примеры неорганических веществ
Неорганические вещества включают в себя различные классы неорганических соединений, включая минералы, соли, кислоты и основания. Вот некоторые примеры неорганических веществ:
1. Вода (H2O) — одно из ключевых неорганических соединений, состоящее из атомов водорода и кислорода.
2. Соль (NaCl) — неорганическое соединение, получаемое из хлористого натрия и хлорида натрия. Является одним из самых распространенных неорганических веществ.
3. Карбонат кальция (CaCO3) — основной компонент мрамора и известняка. Используется в строительстве и производстве цемента.
4. Кислота серной (H2SO4) — является одним из наиболее распространенных неорганических кислот, используется в промышленности для производства удобрений, красителей и других химических соединений.
5. Оксиды (например, оксид железа, Fe2O3) — простые неорганические соединения, состоящие из атомов кислорода и других элементов.
Это лишь некоторые примеры неорганических веществ. Неорганическая химия изучает различные свойства и реакции этих веществ, а их применение широко распространено в различных отраслях науки, медицины и промышленности.
Применение перепревшего навоза
Формирование перегноя
Перепревший навоз, или перегной является основным источником поступления гумуса в почву. Перегной – однородное сыпучее вещество темно-коричневого цвета, с весенним запахом здорового почвенного субстрата. Формируется ферментацией навоза под воздействием микроорганизмов. В результате формируется гумус, гуминовые кислоты и более простые минеральные соединения. По составу перегной легкий. В 1 м³ содержится 700-800 кг перегноя. В стандартном 10 литровом ведре его количество составляет 6-7 кг. Здоровый созревший перегной не имеет запаха.
Свойства перегноя
Перегной обладает следующими агрономическими свойствами:
- улучшает пористость почвы;
- повышает способность удерживать влагу;
- усиливает фотосинтез, чем способствует повышению урожайности сельскохозяйственных культур;
- активизирует рост и развитие растений;
- повышает устойчивость к заболеваниям и поражениям вредителями;
- заселяет почвенный субстрат полезной микрофлорой;
- уменьшает накопление тяжелых металлов в продукции;
- улучшает декоративность цветочных культур и др.
Как приготовить качественный перегной?
- выделяют место в тени для складирования компонентов;
- огораживают подручным материалом так, чтобы передняя стенка была открыта;
- компоненты укладывают послойно, в 10-15 см; компоненты – солома, соломенная резка, листья, навоз свежий, полуперепревший;
- каждый слой проливают водой или разбавленной жижей, раствором коровяка;
- сверху накрывают пленкой или другим материалом, не пропускающим воду (от дождя);
- доступ воздуха через продухи при пленочном укрытии обязателен;
- периодически перелопачивают и в засушливую погоду поливают водой; влажность при ферментации в пределах 50-60%, температура под +25…+30*С;
- для ускорения ферментации рекомендуется проливать слои компонентов препаратами (Байкал ЭМ-1, Экомик урожайный, Сияние-3 и другими).
При выполнении всех требований зрелый перегной можно получить в течение 1-2 месяцев.
Кроме предложенного, есть и другие методы быстрой переработки навоза в перегной или компост, который тоже идет на удобрение и подкормки садово-огородных культур. К примеру, вермикомпостирование с помощью калифорнийских червей, аэробное и анаэробное компостирование.
Качественный и количественный состав веществ
Каждое вещество характеризуется определенным качественным и количественным составом.
Качественный состав вещества показывает, из атомов каких элементов оно состоит. Например, вода состоит из атомов водорода и кислорода, а метан— из атомов углерода и водорода. Число атомов каждого элемента в составе мельчайшей частицы вещества характеризует его количественный состав. Например, молекула воды состоит из двух атомов водорода и одного атома кислорода, а молекула метана — из одного атома углерода и четырех атомов водорода.
Сложное вещество можно с помощью различных химических методов разложить на несколько новых веществ, и так до тех пор, пока не получатся вещества, каждое из которых будет являться простым. Например, сахар при нагревании разлагается на воду и уголь (углерод):
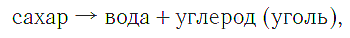
а воду можно разложить с помощью электрического тока на водород и кислород:

Свойства простых веществ, которые при этом получаются (углерода, кислорода и водорода), совершенно не похожи на свойства сложных веществ — сахара и воды. Это разные вещества с разными свойствами. Свойства сложного вещества не являются суммой свойств простых веществ, которые образуются при его разложении.
Сложные вещества, как и простые, имеют либо молекулярное, либо немолекулярное строение. При этом вещества молекулярного строения могут существовать при обычных условиях в различных агрегатных состояниях. Например, метан — газ, вода — жидкость, сахар — твердое вещество.
Вещества немолекулярного строения при обычных условиях — твердые кристаллы, например поваренная соль, мел. Конечно, при нагревании (иногда до нескольких тысяч градусов) такие вещества плавятся, а затем переходят и в парообразное состояние.
Заключение
В заключение следует отметить, что классификация соединений на органические и неорганические зависит от различных факторов. В то время как органические вещества в основном состоят из соединений на основе углерода и изучаются в органической химии, неорганические соединения могут содержать углерод, но сохраняют свою неорганическую природу. Такие примеры, как угольная кислота, соли, получаемые из кислот, цианистый водород и цианиды, демонстрируют существование углеродсодержащих неорганических соединений. Понимая эти различия, мы получаем более глубокое представление об огромном мире химических соединений и их разнообразных характеристиках.
В: В чем разница между органическими и неорганическими веществами? О: Органические вещества – это соединения, которые содержат атомы углерода и изучаются в области органической химии. Неорганические вещества, с другой стороны, могут содержать или не содержать углерод, но не классифицируются как органические соединения. Они изучаются в области неорганической химии.
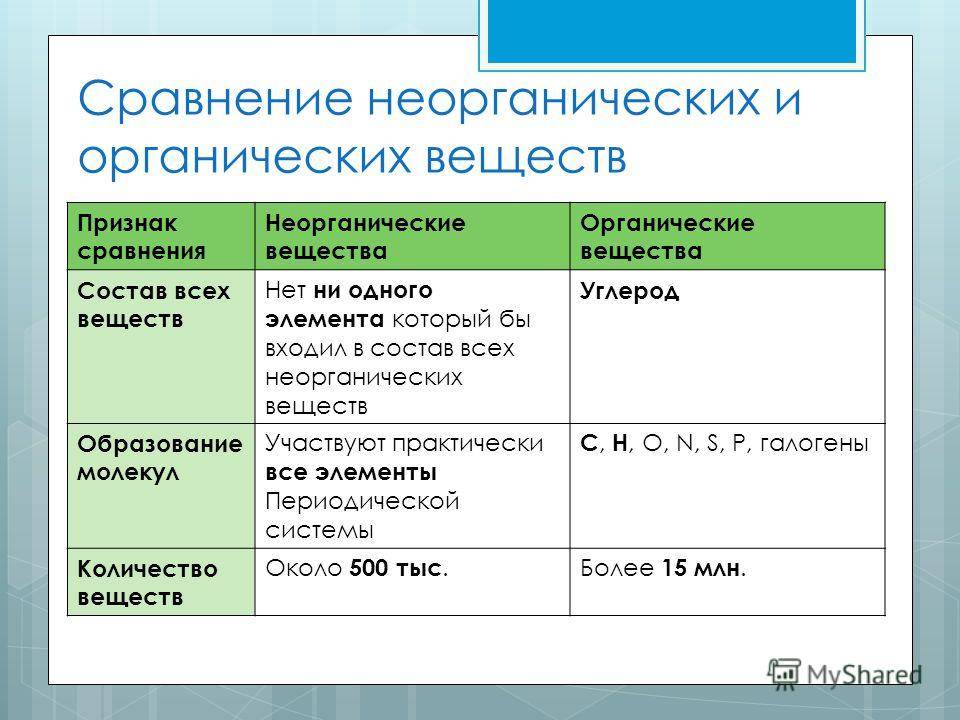
В: Сколько существует известных органических и неорганических соединений? О: Органические соединения более многочисленны, и в настоящее время известно около 40 миллионов органических соединений. В отличие от них, неорганических соединений известно около 700 000.
В: Могут ли неорганические соединения содержать углерод? О: Да, есть исключения, когда неорганические соединения содержат углерод. В качестве примера можно привести угарный газ (CO), двуокись углерода (CO2), угольную кислоту (H2CO3) и некоторые цианиды. Несмотря на содержание углерода, эти соединения все равно считаются неорганическими.
В: Каково значение органической химии? О: Органическая химия имеет решающее значение для понимания и изучения свойств, реакций и применения углеродсодержащих соединений. Она имеет огромное значение в различных областях, таких как фармацевтика, материаловедение, биохимия и экология, что ведет к прогрессу в медицине, технологиях и устойчивых решениях.
В: Каковы некоторые области применения неорганической химии? О: Неорганическая химия находит применение в таких областях, как материаловедение, экология, катализ, хранение энергии и координационная химия. Она вносит вклад в разработку новых материалов, создание катализаторов, понимание экологических процессов и развитие энергетических технологий.
В: Существуют ли какие-либо пересекающиеся области между органической и неорганической химией? О: Да, области органической и неорганической химии могут пересекаться, особенно при изучении металлоорганических соединений. Эти соединения содержат как органические, так и неорганические компоненты и являются предметом междисциплинарных исследований.
Помните, что данный FAQ предназначен для предоставления общей информации, а для более подробных или специфических вопросов рекомендуется обратиться к соответствующей научной литературе или экспертам в данной области.
Что почитать
1. “Органическая химия” Н.Д. Зелинского и А.Е. Фаворского – Этот классический учебник представляет собой полное введение в органическую химию и охватывает различные аспекты органических соединений, их свойства, реакции и применение.
2. “Введение в неорганическую химию” (Введение в неорганическую химию) В.А. Кузнецова – Эта книга предлагает обзор фундаментальных принципов неорганической химии, включая изучение неорганических соединений, их свойств и их применения в различных областях.
3. “Химия: Органическая и неорганическая” (Химия: органическая и неорганическая) А.В. Артемьева и Е.В. Буниной – Учебник представляет собой комплексный подход к органической и неорганической химии, охватывающий основные понятия, реакции и применение органических и неорганических соединений.
4. “Органическая химия: Сборник задач” (Органическая химия: сборник задач) С.А. Чуканова и С.Е. Алексаняна – Эта книга посвящена решению задач по органической химии и содержит сборник упражнений и примеров для углубления понимания предмета и повышения уровня знаний.